Estrategias para combatir enfermedades producidas por la emergencia de resistencia a antibióticos
Strategies to combat antibiotic resistance
María Belén PastrianLa resistencia a los antibióticos constituye, en la actualidad, una de las mayores amenazas para la salud a nivel mundial. Se estima que para el año 2050 la resistencia a los antibióticos presentará un escenario devastador. Como informa Jim O'Neill (2016), ex presidente de la Review on Antimicrobial Resistance, actualmente se producen 700.000 muertes por infecciones resistentes a fármacos vaticinando que se convertirían en 10 millones para la década del 50, es decir, más personas que las que mueren de cáncer.
Los antibióticos son herramientas muy útiles para tratar infecciones y aunque su excesivo e indiscriminado uso genere resistencia, se trata de un proceso evolutivo natural que ha provocado la emergencia de bacterias multirresistentes a los antibióticos.
El manejo terapéutico de las infecciones causadas por microorganismos multirresistentes es cada vez más difícil debido al agotamiento de las alternativas antibióticas. En este contexto, la Organización Mundial de la Salud (OMS), convoca a la comunidad científica y a las empresas farmacéuticas a los fines de aunar esfuerzos en pos del desarrollo de nuevos agentes antimicrobianos que amplíen el arsenal terapéutico para poder responder a este fenómeno a generarse en las próximas décadas.
Resulta fundamental diseñar y desarrollar nuevas entidades cuyo blanco de acción sea un componente celular difícil de modificar o reemplazar para generar resistencia, lo cual constituiría un hallazgo de gran valor para la medicina y la industria farmacéutica.
La comunidad científica ha focalizado su atención en los péptidos antimicrobianos (AMPs) a fin de obtener agentes con aplicación en la producción de alimentos y como agentes terapéuticos. Esto sumado al hecho de que existe poca evidencia de la resistencia microbiana a los AMPs (Peschel, 2006), los convierte en moléculas con gran potencial para su uso como antibióticos. En la actualidad, se conocen más de 2.000 AMPs y su caracterización ha demostrado que la gran mayoría de estos péptidos son catiónicos (péptidos con carga neta positiva).
En este contexto, el fragmento 107 a 115 del extremo C-terminal de la lisozima humana (hLz) posee una actividad antimicrobiana significativa (Iannucci, 2013). En función de lo expuesto se llevó a cabo un trabajo conjunto entre investigadores argentinos (UNQ, UBA y CONICET) y españoles de la Universidad de Barcelona en el que se diseñaron nuevos péptidos que podrían representar excelentes Ingredientes Farmacéuticos Activos (IFAs) para el desarrollo de formulaciones antimicrobianas (González R, 2016), mediante la aplicación de una estrategia novedosa de arilación de péptidos desarrollada por la Universidad de Barcelona con el fin de mejorar la actividad antimicrobiana intrínseca del péptido (Ruiz-Rodríguez J, 2010).
Estos péptidos, denominados momentáneamente KW-Arilados, son péptidos de 9 aminoácidos cuya producción industrial por síntesis química es económicamente rentable. Los potenciales mercados para este desarrollo son las empresas farmacéuticas nacionales y/o internacionales interesadas en responder a la demanda de nuevas entidades antimicrobianas.
Los KW-Arilados son 3 nonapéptidos derivados del fragmento 107-115 de la hLz. Presentan 3 modificaciones respecto a la secuencia líder que aumentaron su actividad antimicrobiana. En la posición 108 se sustituyó la alanina por lisina (Alax Lys), en la posición 111 se sustituyó la alanina por un triptófano (Ala x Trp) (Iannucci, 2013) y se arilaron secuencialmente los 3 Trp de la molécula ubicados en las posiciones 109, 111 y 112 (Rodríguez, 2016). La arilación de Trp se realizó en el carbono 2 con un grupo fenilo con el objetivo de aumentar su capacidad de anclaje en la membrana bacteriana.
La siguiente tabla muestra las secuencias del péptido líder, la secuencia intermedia K108-W111 107-115 hLz y los tres péptidos arilados, cada uno con un Trp-fenilo respectivamente:

Investigaciones previas han revelado que la membrana bacteriana es el blanco de estos péptidos y en ella ejercen su poder destructivo al interrumpir su continuidad, de formarla y crear poros. Este blanco terapéutico implica un difícil desarrollo de resistencia por parte de los microorganismos, constituyendo una virtud adicional de los péptidos KW-Arilados como nuevos agentes antimicrobianos.
La C2-arilación de indoles en Trp se llevó a cabo a través de la técnica de activación del enlace C-H, catalizada por Pd bajo irradiación por microondas (Ruiz-Rodríguez, 2010), como se muestra en la siguiente figura:
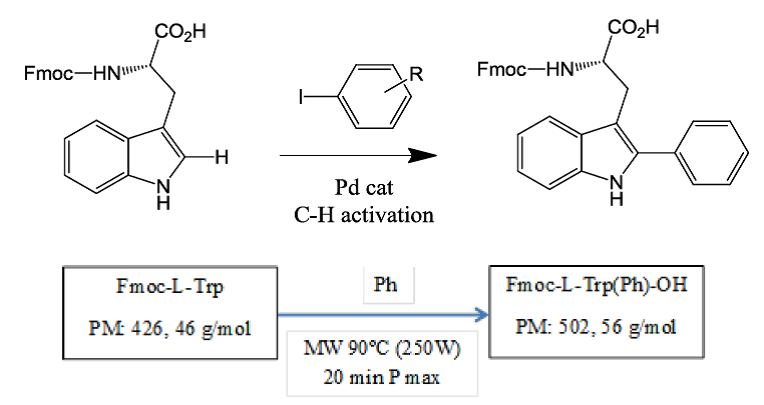
Por lo expuesto, de esta manera se logró potenciar la actividad antimicrobiana de KW-Arilado109, 20 veces frente a un microorganismo Gram negativo (E. coli). Asimismo, se aumentó la actividad antimicrobiana de KW-Arilado111 y KW-Arilado112, 70 veces frente a microorganismos Gram positivos (S. aureus, S. aureus metilino resistente, MRSA y S. epidermidis). La arilación del Trp 109 aumentó selectivamente la actividad del péptido frente a E. coli alcanzando una concentración inhibitoria mínima (CIM) de 20 µM, y ampliando su espectro antimicrobiano. Por otro lado, la arilación de los Trp111 o Trp112, aumentó selectivamente la actividad de los péptidos frente a los microorganismos Gram positivos alcanzando CIMs de 3, 5 y 3 µM frente a S. aureus, MRSA y S. epidermidis respectivamente. Las sustituciones en las posiciones 108 y 111 en el péptido intermediario aumentaron su actividad antimicrobiana 4 y 20 veces frente a microorganismos Gram (-) y Gram (+). Además, la arilación de los Trp aumentó 4 veces la actividad antimicrobiana de los péptidos alcanzando CIMs compatibles con una ventana terapéutica efectiva. La última modificación mejoró el perfil terapéutico de los péptidos, impulsando su candidatura como ingredientes farmacéuticos activos (IFAs) para renovar el arsenal de compuestos antimicrobianos.
La derivatización (arilación) de los Trp a los efectos de aumentar el poder de anclaje de los péptidos a la membrana bacteriana es una técnica novedosa que permitió el hallazgo de los KW-Arilados. Las CIMs obtenidas luego de la derivatización de los Trp, entran en una ventana terapéutica efectiva. Mediante microscopia electrónica, hemos demostrado que la membrana plasmática bacteriana es el blanco de los KW-Arilados; esto implica una baja posibilidad de generación de farmacorresistencia. Asimismo, este blanco terapéutico permitirá el uso de los D-isómeros de los KW-Arilados con el fin de aumentar su estabilidad y biodisponibilidad. Los KW-Arilados puede ser incorporados en varias fórmulas (oral, tópica, inclusión en apósitos, inmovilización en implantes, prótesis y catéteres).
A modo de ejemplo, se muestran fotos obtenidas por microscopía electrónica de barrido que revelan el mecanismo de acción de los péptidos aril-Trp frente a Staphylococcus aureus. La foto de la izquierda representa el control, 0% de inhibición y a la derecha [K108W111W-Ar112] 107-115 hLz, 91% de Inhibición.


Esta significativa innovación podría abrir la puerta a nuevas transformaciones de este tipo, dirigidas a mejorar la acción farmacológica sin alterar la naturaleza anfipática existente del péptido, pero incrementando localmente la lipofilicidad de residuos específicos. De acuerdo a nuestro conocimiento del área, esta es la primera vez que la arilación de un triptófano se aplica en el desarrollo de un péptido con actividad antimicrobiana.
Estos péptidos poseen alta actividad y baja toxicidad, debido a que su blanco terapéutico es la membrana plasmática. Tal y como se mencionó anteriormente, existe una escasa probabilidad de generar resistencia. Considerando que estos péptidos causan daños en la membrana, pueden ser administrados en combinación con un antibiótico que posea un blanco intracelular y de esta forma promover un efecto sinérgico.
A modo de conclusión podemos expresar que los péptidos, ofrecen un potencial de crecimiento enorme como terapias futuras para el tratamiento de las necesidades médicas no cubiertas, anticipando un futuro promisorio para la terapéutica y el diagnóstico.
O´Neill, J. (2016). Tackling drug-resistant infections globally: final report and recommendations. EE.UU: Nature Review Drug Discovery.
González, R., Albericio, F., Cascone, O. y Iannucci, N. (2010). Improved antimicrobial activity of h-lysozyme (107-115) by rational Ala substitution. Journal of Peptide Science, 16, 424-429.
González, R., Mendive-Tapia, L., Pastrian, MB., Albericio, F., Lavilla, R., Cascone, O. y Iannucci, N. (2016). Enhanced antimicrobial activity of a peptide derived from human lysozyme by arylation of its tryptophan residues. Journal of Peptide Science, 22, 123–128.
Iannucci, N., Curto, L., Albericio, F., Cascone, O. y Delfino, J. (2013). Structural Glance Into a Novel Anti-Staphylococcal Peptide. Biopolymers, Peptide Science, 102, 49–57.
Iannucci, N., González, R., Cascone, O. and Albericio, F. (2011). Novel strategy for designing antimicrobial peptides: an answer to the development of drug resistance. Méndez- Vilas (ed.). Science against microbial pathogens: communicating current research and technological advances (pp. 961-967). EE.UU.: Formatex.
Kates, S. A. and Albericio, F. (2000). Solid Phase Synthesis. A Practical Guide. Eds. Marcel Dekker: New York.

