Estudio de Biodiversidad por Técnicas Dependientes e Independientes de Cultivo de una Bodega Ubicada en una Región Re-emergente Argentina
Biodiversity Study by Dependent and Independent Culture Techniques of a Winery located in a Re-emerging Winegrowing Region of Argentina
Eugenia Pose Gabriel A. Rivas Lucrecia DelfedericoLa Argentina se ha ubicado a la vanguardia de la industria vitivinícola gracias a sus sólidas bases en este sector, ubicándose entre los países “top 10” del planeta, siendo el 7º productor mundial de vino (Italia, Francia, España, Estados Unidos, Australia y Chile son los seis primeros), el 8º exportador y el 9º consumidor (OIV, 2021). La superficie de viñedos argentinos se extiende a lo largo de 3.800 km (22º a 45º de latitud sur), desde la Cordillera de los Andes hasta la Pampa húmeda (Chapadmalal, Buenos Aires), y desde la Quebrada de Humahuaca (Jujuy), con viñedos a más de 3.300 metros sobre el nivel del mar, hasta Chubut (45º de latitud sur).
En la provincia de Buenos Aires, la viticultura fue una agroindustria próspera hasta mediados del siglo XX (Ospital, 2003), quedando luego relegada por razones económicas, políticas y sociales. En 1934 se sancionó la ley 12.137, que prohibió toda comercialización de vino procedente de regiones no correspondientes a Cuyo y las provincias cordilleranas del norte. El objetivo era potenciar la actividad vitivinícola de estas regiones, debido a los inconvenientes para cultivar trigo o pasturas para el ganado. Así, esta ley relegó a las demás regiones que estaban en pleno auge de su actividad vitivinícola, incluyendo la provincia de Buenos Aires. Recién en 1997 se modificó esta ley, y sus medidas restrictivas se relajaron paulatinamente, permitiendo la recuperación de la vitivinicultura bonaerense a través de emprendimientos que hoy muestran diferentes grados de desarrollo (Ospital, 2019).
La elaboración del vino es un proceso complejo que implica dos fermentaciones sucesivas: la fermentación alcohólica (FA), llevada a cabo por levaduras, y la fermentación maloláctica (FML), por bacterias ácido-lácticas (BAL). La FML es un paso importante porque involucra la conversión del ácido L-málico en ácido L-láctico, conducente a una deseable reducción en la acidez y astringencia. Las especies más relevantes en enología son Oenococcus oeni y Lactiplantibacillus plantarum. Ambas demostraron en numerosos trabajos ser capaces de resistir a las condiciones estresantes del vino (como la acidez, escasez de nutrientes, elevada concentración de etanol), presentar una gran eficiencia en el consumo del ácido málico, y poseer variadas actividades enzimáticas secundarias que les permiten sintetizar o modificar otros compuestos que aportan al color, sabor, textura y aroma del vino (Bartowsky 2005; Betteridge, Grbin, & Jiranek, 2015; Borneman, McCarthy, Chambers, & Bartowsky, 2012; Bravo-Ferrada et al., 2013; du Toit, Engelbrecht, Lerm, & Krieger-Weber, 2011; Krieger-Weber, Heras, & Suarez, 2020; Swiegers & Pretorius, 2005; Virdis, Sumby, Bartowsky, & Jiranek, 2021).
Las técnicas dependientes de cultivo resultan indispensables para el aislamiento, identificación y caracterización de BAL. A su vez, esto es necesario con el objeto de seleccionar aquellas que tengan las mejores propiedades tecnológicas y enológicas a fin de ser utilizadas en la formulación de cultivos iniciadores de fermentación maloláctica. La transferencia tecnológica al sector productivo permitiría la utilización de estos iniciadores a nivel regional o en regiones vitivinícolas con características similares. Sin embargo, las técnicas dependientes de cultivo no resultan suficiente o adecuadas para caracterizar la compleja biodiversidad presente en el vino, principalmente debido a las limitaciones actuales para el crecimiento de todos los microorganismos presentes en una muestra (Montgomery, 2020; Stewart, 2012). Por lo que, técnicas independientes de cultivo, y en especial, las técnicas de secuenciación de próxima generación (NGS), se utilizan a menudo para caracterizar mejor la diversidad microbiana de ecosistemas complejos; que desempeñan un papel clave en el cultivo de uvas para vinificación (Vitis vinifera), la producción y la calidad del vino (D. Liu, Zhang, Chen, & Howell, 2019). También posibilitan la detección de microorganismos que pudieran estar en un estado de viables no-cultivables (VNC), en el cual muchas BAL pueden encontrarse cuando las condiciones del entorno resultan estresantes (como la elevada concentración de etanol, presencia de sulfito, etc.), y por lo cual, se puede dificultar en gran medida su detección por técnicas dependientes de cultivo (Capozzi et al., 2016; Kioroglou, 2020; Millet & Lonvaud‐Funel, 2000) .
Recientemente, otros autores comenzaron a evaluar la diversidad de comunidades microbianas asociadas a viñedos argentinos aplicando NGS (Oyuela Aguilar et al., 2020; Paolinelli et al., 2023; Vega-Avila et al., 2015), sin embargo, dichos estudios se centraron en las regiones vitivinícolas más tradicionales del país. Regiones re-emergentes, como la bonaerense, permanecen sin estudiar o cuentan con escasos trabajos que aborden el estudio de sus estructuras microbianas y del proceso de fermentación de sus vinos. En el caso de la Provincia de Buenos Aires, el sector vitivinícola se está desarrollando de una manera acelerada y, aunque contribuye minoritariamente a la producción del país, cobra cada vez más relevancia, mejorando la calidad de sus vinos con un terroir único, ampliando variedades y exportando sus productos (INV, 2021), razón por la cual en los últimos años nos hemos enfocado en estudiar dicha región.
En estudios previos hemos comparado la diversidad fúngica y bacteriana del suelo y rizósfera, para la vendimia 2017, entre dos bodegas bonaerenses, bodegas Al-Este y Saldungaray. En dicho trabajo se observó que las estructuras microbianas resultaron ser muy similares, encontrando únicamente diferencias significativas al analizar grupos de microrganismos en niveles taxonómicos específicos (Rivas, Semorile, & Delfederico, 2022). También hemos estudiado por NGS, la influencia del clima a lo largo de 3 vendimias consecutivas (2017-2019) en la biodiversidad del suelo y vino para la bodega Saldungaray, advirtiendo la escasez o ausencia de BAL en muestras de mosto y vino, además, observando que el suelo no estaría actuando de reservorio biológico de este grupo microbiano relevante en enología. Adicionalmente, la escasez o ausencia de BAL encontrada podría estar relacionada con la ralentización en la FML reportada previamente por el enólogo de la bodega, la cual en caso de que ocurra, es llevada a cabo de forma espontánea ya que la bodega no utiliza iniciadores de FML comerciales (Rivas, Guillade, Semorile, & Delfederico, 2021). Sin embargo, hasta el momento no se han realizado estudios de regiones re-emergentes argentinas que comparen análisis de biodiversidad mediante técnicas dependientes e independientes de cultivo. Por lo que, el objetivo del presente trabajo consistió en estudiar una muestra de mosto de la vendimia 2018 de la bodega Saldungaray (SO de la Provincia de Buenos Aires), mediante técnicas dependientes e independientes de cultivo, con especial énfasis en la comparación de las BAL detectadas por dichos abordajes.
2.1 Región de estudio y muestreo:
La bodega Saldungaray se ubica en un sitio estratégico, correspondiente a la zona de transición entre las regiones fitogeográficas Pampeana y Espinal (Cabrera, 1976). Se encuentra en producción desde 2003, y posee 20 ha cultivadas con varietales Chardonnay Sauvignon Blanc, Malbec, Merlot, Cabernet Sauvignon, Pinot Noir y Cabernet Franc. La cuadrícula de plantación corresponde a hileras separadas 2 m y vides separadas 1 m, conducidas en un brote en posición vertical. El sistema de poda es cordón de Royat bilateral, con el suelo entre hileras cubierto de hierba autóctona. El agua superficial se distribuye por un sistema de riego por goteo basado en agua subterránea de un acuífero. Dicho sistema y un ventilador anti-escarcha colocado en una esquina de la parcela, protegen al viñedo del daño por heladas. El manejo de plagas y enfermedades involucra uso de herbicidas (glifosato Round-up®) y fungicidas (Captan®, Folpet®, Mancozeb®, Ziram® y Zineb®).
La bodega produce principalmente vinos jóvenes (sin añejamiento). El proceso de vinificación comienza con la selección de la uva de forma manual, y se coloca en depósitos de fermentación de acero u hormigón. El proceso inicia con una pre-fermentación en frío durante 48-72 h. La FA involucra el uso de la levadura comercial Uvaferm BC® (Lallemand Inc., Montréal, QC, Canadá) como iniciador, y se completa en unos 10 días. Luego de un prensado, se deja que ocurra una FML espontánea durante 25 a 40 días. Cabe destacar que en esta bodega nunca se emplearon iniciadores malolácticos y que los enólogos de la misma reportaron una desaceleración de la FML a lo largo de los años.
La bodega Saldungaray se ubica en la denominada “diagonal árida argentina”, una franja de tierra escasamente pluviométrica que se extiende desde el norte del Perú hasta el litoral atlántico patagónico. El clima es templado semiárido, con marcada estacionalidad en las precipitaciones, que ocurren en primavera y otoño (A. Campo, Ramos, & Zapperi, 2009) y con vientos moderados a fuertes todo el año, principalmente del oeste, y particularmente intensos desde finales de primavera hasta mediados de verano. Otra particularidad de la zona son los eventos meteorológicos extremos, como granizo, heladas, sequías e inundaciones, que ocurren en patrones cíclicos (A. M. Campo, Gil, Gentili, Volonté, & Duval, 2011). El resultado de las características climáticas descriptas es una limitada disponibilidad de agua subterránea para los sistemas de riego.
Por otro lado, en 2018, la bodega reportó una gran disminución en la producción de uva debido a heladas fuera de estación (primavera), resultando un rendimiento insuficiente para la producción de vinos de cada varietal. En consecuencia, se obtuvo una muestra de mosto de uva, mezcla de varietales Malbec, Pinot Noir, Chardonnay y Cabernet Sauvignon que fue el objeto de estudio del presente trabajo. Este mosto se utilizó como base para la elaboración del vino espumoso de ese año, que la bodega produce habitualmente a partir de Pinot Noir.
2.2 Análisis de BAL por técnicas dependientes de cultivo:
2.2.1 Aislamientos:
El mosto se filtró mediante filtros de 0.45 µm a fin de eliminar o reducir el número de levaduras. Posteriormente, se realizaron varios ciclos de enriquecimiento en caldos MRS (Mann Rogosa y Sharpe; Britania, CABA, Argentina) y MLO, suplementados con nistatina (20 mg/L) y cicloheximida (20 mg/L), agregadas para inhibir el crecimiento de levaduras. En cada ciclo se incubó 1 mL de mosto, o del enriquecimiento anterior, en 9 mL de medio, durante 7 días a 28 °C, en condiciones de microaerofilia. Posteriormente, utilizando espátula de Drigalsky, se hicieron siembras en agar MRS y MLO, en idénticas condiciones. Se obtuvieron cultivos axénicos mediante sucesivas estrías por agotamiento. Los cultivos puros se sometieron a pruebas de catalasa y a observación microscópica con tinción de Gram. Como posibles BAL, se seleccionaron los aislamientos Gram positivos, no esporulantes, catalasa negativos.
2.2.2 Extracción de ADN:
Los aislamientos se crecieron durante 72 h (28 °C, microaerofilia) en el medio correspondiente (MRS o MLO, según procedencia de cada aislamiento), para extraer ADN genómico según Bravo-Ferrada et al. (2013). La integridad y calidad del ADN obtenido se evaluó mediante electroforesis en gel de agarosa 1%, teñido con GelRed (Sigma-Aldrich) y por medición de las absorbancias a 260, 280 y 230 nm nanodrop (NanoDrop® ND-1000 Thermo Scientific).
2.2.3 Identificación:
Los aislamientos fueron identificados a nivel de especie mediante secuenciación de un fragmento del gen de 16S rRNA, con los primers pA16SF y pH16SR (Rodas, Ferrer, & Pardo, 2003) y comparación de las secuencias con base de datos (GenBank del NCBI).
2.2.4 Tipificación:
Cada aislamiento se tipificó molecularmente a nivel de cepa, mediante Random Amplified Polymorphic-DNA (RAPD-PCR) (Williams, Kubelik, Livak, Rafalski, & Tingey, 1990), con el primer M13 (Stenlid, Karlsson, & Högberg, 1994), según Delfederico et al. (2006).
2.2.5 Cinéticas de crecimiento y resistencia al etanol
A fin de evaluar el comportamiento de las cepas salvajes en presencia de diferentes concentraciones de etanol, se compararon las cinéticas de crecimientos en medio de cultivo respecto del crecimiento en medio de cultivo suplementado con etanol. Las cepas se cultivaron en los medios MLO o MRS según correspondiera, se estandarizaron los inóculos a una DO de 0.5, y se inocularon al 10%, por triplicado, en placas de 96 wells, ensayando las condiciones: I- Medio sin suplementar, II- Medio + 6% etanol, III- Medio + etanol 12%. La placa de 96 wells fue incubada a 28°C y se realizaron mediciones (DO600) con un lector de placas (BioTek Synergy HTX) a lo largo del tiempo. Los gráficos se realizaron utilizando Graphpad 6.0.
2.3 Análisis de biodiversidad por técnicas independientes de cultivo:
2.3.1 Estandarización de protocolo de extracción de ADN genómico total:
Se centrifugaron alícuotas de 35 mL de muestra de mosto durante 15 min a 8.000 rpm, los pellets se lavaron dos veces con buffer Tris-EDTA (TE) (20:2 mM) y luego se resuspendieron en 1 mL de PBS cada una. La extracción de ADN se realizó con el FastDNA Spin Kit for Soil (MP Biomedicals). Las condiciones de la extracción de ADN requirieron modificaciones del protocolo sugerido por el fabricante, que consistieron en modificar las condiciones de la digestión mecánica mediante la agitación de beads (perlas) con un bead-beater y/o agregar acción enzimática con lisozima. Los pellets fueron resuspendidos en buffer de lisis MT (provisto por el kit) y las condiciones de extracción de ADN ensayadas fueron: A. Tratamiento con lisozima 15' a 37°C y ciclo de 5' de agitación; B. Tratamiento con lisozima 30' a 37 °C, y ciclo de 5' de agitación; C. Un ciclo de 5' de agitación, e incubación con lisozima 30'; D. Un ciclo de 5’ de agitación; E. Dos ciclos de 1' 30'' de agitación, con recuperación de sobrenadante entre ciclo; F. Dos ciclos de 1' 10'' 30'' de agitación, con incubación de 2' de hielo entre cada ciclo. Adicionalmente, se agregó un paso de clarificación luego de la precipitación de proteínas y otros detritus, agregando polivinilpolipirrolidona (PVPP) 10% p/v, mezclando con vórtex, y posteriormente centrifugando durante 10 min a 14000 g.
2.3.2 Análisis de calidad del material genético:
A fin de revelar cuál de los protocolos realizados resultó el más adecuado, la calidad e integridad del DNA obtenido se visualizó en un gel de agarosa 1%, teñido con bromuro de etidio (0,5 mg/mL), en presencia de un ladder de 1 Kpb (PB-L Productos Bio-Lógicos). Mediante un equipo Nanodrop se evaluó la concentración y la pureza del ADN obtenido, midiendo la absorbancia a 230, 260 y 280, utilizando como criterios mínimos: una concentración de 20 ng/mL o superior, una relación 260/280 entre 1,7-2,1, y una relación 260/230 entre 1,5-2,1.
2.3.3 Estudio de diversidad por secuenciación masiva:
Las muestras de ADN genómico se enviaron a Macrogen Korea (Seúl, República de Corea), donde se realizó la amplificación masiva del gen 16S rRNA. Para ello se prepararon las bibliotecas de amplicones (Herculase II Fusion DNA Polymerase Nextera XT Index Kit V2). La región hipervariable V3-V4 del gen 16S rRNA, obtenida utilizando los primers Bakt_341F: 5′-CCTACGGGNGGCWGCAG-30 y Bakt_805R: 5′-GACTACHVGGGTATCTAATCC-30, fue secuenciada por Illumina (MiSeq). Se obtuvieron secuencias apareadas de 301 pb de longitud. Los datos de la secuencia se depositaron en NCBI (bioproyecto PRJNA742427) (Rivas et al., 2021).
2.3.4 Análisis de las secuencias
Brevemente, el análisis se realizó utilizando QIIME2 (Callahan et al., 2016) tal y como se describió en Rivas et al. (2021). Las secuencias fueron depuradas de secuencias quiméricas, de baja calidad. También las regiones de baja calidad de los extremos fueron recortadas y las secuencias correspondientes a cloroplastos eliminadas (McDonald, Clemente, et al., 2012; McDonald, Price, et al., 2012). Se realizó el análisis taxonómico utilizando la base de datos de Greengenes (v13) (DeSantis et al., 2006). Para el presente trabajo, los resultados se utilizaron para comparar la diversidad microbiana obtenida mediante técnicas dependientes e independientes de cultivo .
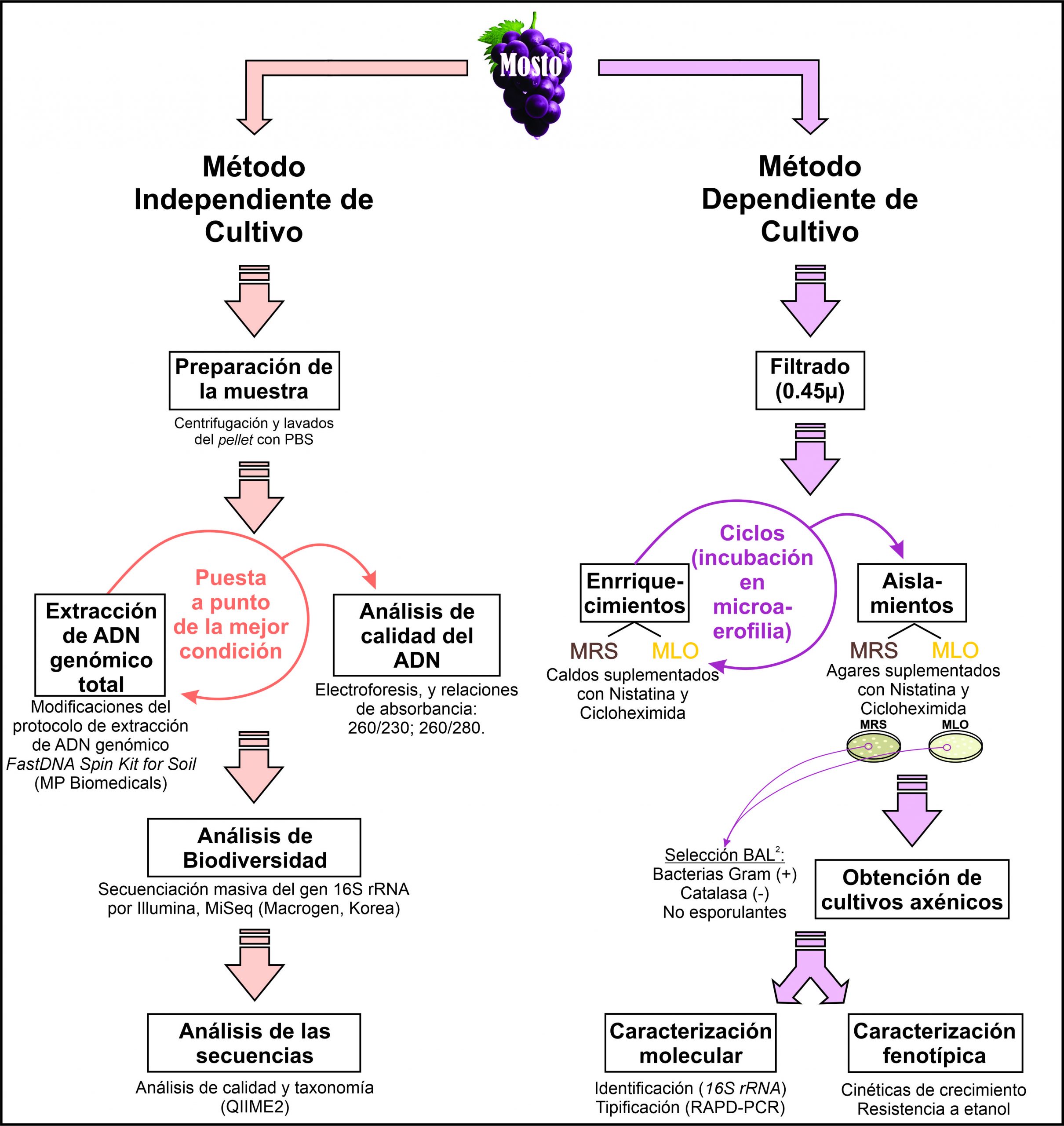
3.1 Análisis de BAL por técnicas dependientes de cultivo:
A partir de sucesivos ciclos de enriquecimientos y siembra en los medios MRS y MLO, se lograron obtener 18 aislamientos de bacterias Gram positivas, catalasa negativas, presuntivamente identificadas como BAL. Se realizó un screening de los aislamientos mediante tipificación por RAPD-PCR, hallando un total de 6 cepas con perfiles electroforéticos únicos. Dichas cepas se identificaron a nivel de especie por amplificación y secuenciación del gen de 16S rRNA. Luego, las mismas se compararon con la base de datos de Genbank (NCBI, NIH), identificándose 4 cepas de Lactiplantibacillus plantarum, 1 de Enterococcus mundtii y 1 de Enterococcus durans (Figura 2).
A fin de realizar una primera caracterización y evaluar si resultasen buenas candidatas para la posible formulación de un iniciador de fermentación maloláctica autóctono, se estudiaron sus cinéticas de crecimiento y resistencia al etanol (6 y 12%) (Figura 3, A-D). Todas las cepas de Lpb. plantarum mostraron una buena resistencia de crecimiento a las concentraciones de etanol ensayadas, creciendo rápidamente en las primeras 24 h y luego manteniendo la biomasa. La cepa C8 alcanzó una biomasa final de alrededor de 7x108 UFC/mL y parece haber sido la única que creció igual independientemente de las condiciones (sin etanol, etanol al 6 o 12%), mientras que, las demás habrían tenido una leve ralentización de crecimiento durante la fase exponencial en la condición con etanol 12%. Adicionalmente, la cepa C10 fue la que alcanzó una biomasa mayor, de alrededor de 7,6 x108 UFC/mL.
Por otra parte, las cepas de E. mundtii C12 y E. durans C14 mostraron un comportamiento variable en sus cinéticas de crecimiento (Figura 3, E-F), alcanzando una biomasa final cercana a 1.4x108 UFC/mL. Dicha biomasa fue alcanzada entorno a las 24 h de crecimiento para las condiciones sin etanol y etanol al 6%. Mientras que la condición de 12% etanol parece haber producido una ralentización en su crecimiento. Sin embargo, ambas especies lograron alcanzar una biomasa similar al cabo de las 72 h.
3.2 Análisis de biodiversidad por técnicas independientes de cultivo:
A fin de realizar el análisis de biodiversidad por secuenciación masiva del gen 16S rRNA (Illumina, MiSeq), la muestra de mosto fue previamente procesada y se procedió a la optimización del protocolo de extracción de ADN genómico total utilizando distintas estrategias. Las mismas consistieron en variar los tiempos de exposición de dos posibles tipos de extracción de ADN: una extracción mecánica, mediante la agitación de pequeñas esferas (beads) con un bead-beater, y/o una extracción enzimática con lisozima (Materiales y Métodos 2.3.1).
En la Figura 4 se muestra la calidad de ADN obtenido mediante cada estrategia empleada, pudiéndose observar que la estrategia F, que involucró dos ciclos de lisis mecánica de 1’ 10’’, y con incubación de 2’ de hielo entre cada ciclo, fue la que permitió obtener un ADN con la mayor intensidad de banda y el menor nivel de degradación. Asimismo, las otras dos estrategias que involucraron digestión mecánica mostraron mayor nivel de degradación y una disminución en la intensidad (estrategia E), o intensidad similar de banda, pero mayor nivel de degradación (estrategia D). Por otra parte, la estrategia A que involucró 15’ de incubación con lisozima y 5’ de digestión mecánica, mostró resultados de degradación e intensidad de banda similares a la estrategia D. Mientras que las estrategias B y C, que involucraron mayor tiempo de exposición con la lisozima, dio como resultado un ADN degradado casi por completo.
La muestra de ADN obtenida mediante la estrategia F fue enviada a Macrogen (Korea), donde se realizó la biblioteca y la secuenciación masiva de la región V3-V4 del gen de 16S rRNA mediante Illumina (MiSeq), obteniéndose un total de 180310 lecturas. Luego del proceso de la eliminación de secuencias y regiones de baja calidad, así como de aquellas que se correspondieron con secuencias quiméricas, cloroplastos y mitocondrias, se obtuvieron un total de 3531 unidades taxonómicas operativas (UTOs).
Mediante un análisis taxonómico, se observó que, a nivel de filo, las Proteobacterias con un 56,40% fueron el grupo con mayor abundancia relativa, seguida de las Actinobacterias con un 20,30% y por los Firmicutes con un 19,58%. El porcentaje restante estuvo constituido por grupos como Chloroflexe, Planctomycetes y otras secuencias minoritarias y sin identificar (Figura 5-A).
Debido a que las BAL, el grupo de bacterias más relevantes en enología, pertenecen al filo Firmicutes, se realizó un análisis del mismo con mayor profundidad. En la Figura 5-B, se muestra el nivel taxonómico de Orden al que se llegó por esta técnica independiente de cultivo para dicho filo, y se observó que únicamente se encontraron los órdenes Bacillales y Clostridiales, no habiéndose detectado el orden Lactobacillales al cual pertenecen las BAL.
Discusión:
En el presente trabajo, se abordó un análisis de biodiversidad de una muestra de mosto de la vendimia 2018 de la Bodega Saldungaray (Buenos Aires), seleccionada debido a que se encuentra ubicada en una de las regiones vitivinícolas re-emergentes, escasamente estudiada de nuestro país. El análisis consistió en comparar los resultados obtenidos por técnicas dependientes e independientes de cultivo, con especial énfasis en las BAL, grupo microbiano de gran relevancia enológica debido a que son las encargadas de realizar la conversión del ácido L-málico en ácido L-láctico (FML), conducente a una deseable reducción en la acidez y astringencia del vino (Krieger-Weber et al., 2020).
Mediante las técnicas dependientes de cultivo se lograron aislar, identificar (por secuenciación del gen de 16S rRNA) y tipificar (por RAPD-PCR), 6 cepas diferentes: 4 de Lpb. plantarum, 1 de E. mundtii y 1 de E. durans. Si bien las especies de Enterococcus fueron también caracterizadas, el rol de este género en las matrices alimentarias, incluidas el vino, suele ser controversial y no se suelen asociar con microorganismos de relevancia enológica. Además, cabe mencionar que las especies encontradas en este trabajo no son las usualmente detectadas en vino, ya que en general la especie que se suele aislar es E. faecium (Capozzi et al., 2011; Pérez-Martín, Seseña, Izquierdo, & Palop, 2014). Por el contrario, Lpb. plantarum es una de las BAL frecuentemente aisladas y reconocida a nivel mundial por llevar a cabo FML exitosas debido a su capacidad de dominar el proceso fermentativo, conduciendo a un elevado y rápido consumo de ácido L-málico (Bravo-Ferrada et al., 2013; du Toit et al., 2011; Krieger-Weber et al., 2020). Esto es posible gracias a la capacidad de las BAL de tolerar las condiciones del vino como, la presencia de SO2, y la producción y liberación de ácidos grasos, péptidos, polisacáridos y otras moléculas por parte de las levaduras, que pueden alterar el crecimiento bacteriano y el normal desarrollo de la FML (Jin, Jiranek, Hayes, & Grbin, 2022; Ngwenya, Nkambule, & Kidane, 2023; Tedesco et al., 2022; Xu et al., 2021). El aislamiento de las BAL obtenidas por técnicas dependientes de cultivo resulta insuficiente para caracterizar la compleja biodiversidad presente en el vino, principalmente debido a la actual imposibilidad de aislar todos los microrganismos presentes (Montgomery, 2020; Stewart, 2012). Sin embargo, resultan indispensables para el aislamiento, identificación y caracterización de este grupo microbiano de relevancia enológica. Lo cual, a su vez, es necesario a fin de seleccionar aquellas que tengan las mejores propiedades tecnológicas y enológicas a fin de poder ser utilizadas en la formulación de cultivos iniciadores de fermentación maloláctica.
La caracterización inicial de las cepas de Lpb. plantarum obtenidas mediante sus cinéticas de crecimiento en presencia de diferentes concentraciones de etanol (6 y 12%), sugirió una elevada resistencia al etanol en las condiciones ensayadas, lo que nos permite pensar en dichas cepas como promisorias para la formulación de iniciadores malolácticos, aunque se requiere una caracterización tecnológica más profunda de las mismas. Otros autores han realizado distintas investigaciones que se enfocaron en el uso de Lpb. plantarum para conducir la FML, obteniendo muy buenos resultados (Berbegal et al., 2016; Bravo-Ferrada et al., 2013; Bravo‐Ferrada, Tymczyszyn, Gómez‐Zavaglia, & Semorile, 2014; du Toit et al., 2011; Iorizzo et al., 2016; Lerm, Engelbrecht, & Du Toit, 2011; Lucio, Pardo, Krieger-Weber, Heras, & Ferrer, 2016) . Se ha demostrado que cepas de esta especie, además de la enzima maloláctica, poseen variadas actividades enzimáticas secundarias que les permiten sintetizar o modificar otros compuestos, que aportan al color, sabor, textura y aroma, mejorando las características organolépticas de los vinos (Brizuela et al., 2021; Cao et al., 2022; Krieger-Weber et al., 2020; Liu, 2002; Virdis et al., 2021).
Los cultivos iniciadores o starters constituyen una innovación fundamental para el sector vitivinícola. Si bien resulta posible controlar el inicio y progresión de la FML por inoculación de cepas seleccionadas de BAL, esta fermentación puede ocurrir de manera espontánea si las condiciones son favorables. Sin embargo, la FML espontánea implica riesgos, como un considerable incremento en la acidez volátil, el consumo de azúcares residuales y la formación de metabolitos indeseables como aminas biogénicas (AB) y etilcarbamato (EC), que afectan la salud humana y conducen a vinos de baja calidad (Spano et al., 2010). Además de Lpb. plantarum, otra especie de gran relevancia enológica es Oenococcus oeni, reconocida por su gran resistencia al etanol y una actividad metabólica capaz de modificar las propiedades organolépticas del vino (Bartowsky 2005; Bartowsky & Borneman, 2011; Lorentzen & Lucas, 2019). A pesar de haber intentado buscarla, en el presente trabajo no hemos logrado aislar ninguna cepa de dicha especie. Adicionalmente, cabe mencionar que el uso de iniciadores de fermentación maloláctica constituidos por cepas autóctonas contribuyen a la conservación del terroir característico del vino de origen. Por lo tanto, destacamos la relevancia de trabajos como el presente, que permiten el incremento de cepas autóctonas disponibles de gran importancia para la vitivinicultura regional, con la potencialidad de lograr adaptarse y comercializarse a regiones vitivinícolas con características similares.
Por otra parte, las técnicas de secuenciación masiva, independientes de cultivo, son también de gran relevancia. Estas permiten estudiar las comunidades microbianas con un elevado nivel de profundidad, con posibilidad de detectar otros grupos microbianos que pudieran ser relevantes para el proceso fermentativo y la calidad del vino. También posibilitan la detección de microorganismos que pudieran estar en un estado de viables no-cultivables (VNC), en el cual muchas BAL pueden encontrarse cuando las condiciones del entorno resultan estresantes (elevada concentración de etanol, presencia de sulfito, etc.), y por lo cual, se puede dificultar en gran medida su detección por técnicas dependientes de cultivo (Capozzi et al., 2016; Kioroglou, 2020; Millet & Lonvaud‐Funel, 2000) . Esto último, podría ser una explicación posible por la cual, a pesar de los sucesivos ciclos de enriquecimientos y aislamientos en dos medios de cultivos diferentes (MRS y MLO), no hemos sido capaces de aislar cepas de O. oeni.
El proceso extracción de ADN genómico total resulta un paso crítico para los análisis de biodiversidad por técnicas independientes de cultivo, ya que los resultados posteriores dependerán del éxito de esto, pudiendo alterar la abundancia relativa de los microorganismos detectados. Las muestras de mosto tienen aparejados a su vez dos dificultades: por un lado, la necesidad de concentrar la muestra para incrementar la sensibilidad en la detección de los microorganismos. Por otro lado, es de gran importancia evitar contaminaciones con ciertos compuestos, como los polifenoles, muy abundantes en estos tipos de muestras, ya que los mismos pueden actuar como inhibidores en las reacciones de PCR posteriores que son necesarias tanto para el armado de las bibliotecas como para el proceso de secuenciación por síntesis, como es el caso de Illumina (Gobert, Evers, Morge, Sparrow, & Delafont, 2022; Işçi, Kalkan Yildirim, & Altindisli, 2014). Por esta razón, resultó de gran importancia la optimización del protocolo provisto por el fabricante del kit FastDNA Spin Kit for Soil (MP Biomedicals), siendo que el proceso debe ser lo suficientemente potente como para lograr la ruptura de diferentes tipos de pared celular bacterianas, pero no demasiado potente, como para causar una excesiva degradación del ADN genómico total. Dicho equilibrio pareciera haber sido el caso con la estrategia F en el presente trabajo, que involucró únicamente dos ciclos de digestión mecánica, sin actividad enzimática; seguida de la estrategia E, y luego la estrategia D. De acuerdo con los resultados obtenidos, el agregado de un paso de lisis enzimática resultó ser excesiva, provocando la lisis completa del material genético, como se observó con las estrategias B y C. La estrategia A, sería una excepción, en donde se observó un resultado similar a la estrategia D que involucraba únicamente digestión mecánica. Probablemente debido a que la estrategia A involucraba la mitad de tiempo de exposición con la enzima respecto de las estrategias B y C.
Hay pocos trabajos que analicen la efectividad y el impacto de distintos tipos de extracción de ADN, realizando los análisis de biodiversidad por técnicas de secuenciación masiva a partir del ADN genómico obtenido con cada uno de ellos (Gobert et al., 2022; Hall, Cadle-Davidson, Fang, & Wilcox, 2019; Jara, Mateo, Guillamón, Torija, & Mas, 2008). Sin embargo, de acuerdo con nuestro conocimiento, en ninguno de éstos se utilizó el kit utilizado en el presente trabajo o plantean modificaciones ad hoc a partir de los protocolos provistos por los fabricantes, por lo que los resultados aquí presentados podrían contribuir a la literatura actual. Siendo relevante realizar a futuro un análisis comparativo de biodiversidad a partir de diferentes modificaciones del protocolo, para evaluar su impacto en los resultados al final de la secuenciación masiva de amplicones, como la sensibilidad de detección en grupos taxonómicos específicos.
Los resultados obtenidos en el presente trabajo mediante la secuenciación masiva de la región V3-V4 del gen 16S rRNA con Illumina (MiSeq), coinciden con los encontrados por otros autores que identifican, en muestras de mosto y vino, a nivel de filo, al grupo Proteobacterias como las más abundantes, seguidas de Actinobacterias y Firmicutes (Bokulich, Thorngate, Richardson, & Mills, 2014; del Carmen Portillo & Mas, 2016; Morgan, Du Toit, & Setati, 2017; Pinto et al., 2015; Pinto et al., 2014). También resultan consistentes con los obtenidos previamente para la bodega Saldungaray en las vendimias 2017 y 2019 (Rivas et al., 2021; Rivas et al., 2022). Como se mencionó anteriormente, aún con un análisis taxonómico más profundo de los resultados obtenidos por NGS del filo Firmicutes, no se logró la detección del orden Lactobacilalles, al que pertenecen las BAL. No obstante, con estrategias de enriquecimiento y varias rondas de aislamientos se obtuvieron diferentes cepas de BAL, lo cual nos conduce a suponer que las BAL se encontraban en concentraciones tan bajas que dificultaron su detección por la técnica independiente de cultivo empleada. El hecho de que <0,1% del genoma total son genes ribosómicos, dificulta la amplificación de este marcador a partir de genomas muy poco abundantes en una muestra (Escobar-Zepeda, Vera-Ponce de León, & Sanchez-Flores, 2015). Esto a su vez, resulta parcialmente consistente con resultados para otras vendimias en la bodega Saldungaray, siendo que para la vendimia 2019, tampoco se logró encontrar ningún miembro del orden Lactobacillales; mientras que para la vendimia 2017 se lograron encontrar, pero con abundancias relativas inferiores al 1% (Rivas et al., 2021; Rivas et al., 2022), aunque en ninguno de estos trabajos se abordaron estrategias dependientes de cultivo. Asimismo, además de la posible escasez de BAL en la muestra de mosto 2018, la dificultad de detección de las mismas también podría explicarse por la presencia de regiones de alta/baja calidad en las secuencias, que afectarían la efectividad de discriminación durante la clasificación taxonómica. Estas regiones de mayor o menor calidad podrían deberse a la eficiencia de la reacción de PCR y del proceso de amplificación, debido a disparidades en secuencia y longitud del target, contenido de GC, y mismatch con los primers (Takahashi, Kita, Mizuno, & Goto-Yamamoto, 2017), introduciendo un sesgo de identificación taxonómica. Para corroborarlo, algunas estrategias posibles podrían ser: I. Utilizar primers dirigidos a otra región hipervariable del gen de 16S rRNA (V1-V9); II. Utilizar primers dirigidos a otro gen housekeeping; III. Cambiar de tecnología de secuenciación a una de tercera generación como PACBIO que, a pesar de ser mucho más costosa económicamente, admite la secuenciación de amplicones más grandes, pudiendo secuenciar el gen de 16S rRNA completo, lo cual podría favorecer la detección de genomas con escazas abundancias relativas (Escobar-Zepeda et al., 2015; Fichot & Norman, 2013).
En el presente trabajo se logró aislar, identificar y tipificar 6 cepas diferentes de BAL, entre las que se encontraron 4 cepas de relevancia enológica (Lpb. plantarum). Sus cinéticas de crecimiento y resistencia a la presencia de diferentes concentraciones de etanol permitieron sugerir su posible resistencia al entorno vino y el proceso fermentativo, siendo candidatos promisorios a fin de formular iniciadores malolácticos autóctonos que pudieran ser comercializados a la misma región y, posiblemente, a regiones de características similares. Por otra parte, fue posible realizar la optimización del proceso de extracción de ADN genómico total con características adecuadas para el estudio por técnicas independientes de cultivo como la secuenciación masiva (NGS) por Illumina. Estos análisis permitieron caracterizar la estructura microbiana de muestras cuya composición resulta un desafío.
Los resultados obtenidos demuestran la necesidad de abordar el estudio de poblaciones microbianas con intereses biotecnológicos de una forma integral, mediante técnicas dependientes e independientes de cultivo, entendiendo cuales son las virtudes y desventajas de cada estrategia empleada. El presente trabajo posee un elevado interés regional, y refuerza la necesidad de continuar estudiando viñedos y bodegas ubicadas en regiones re-emergentes de la Argentina, que debido a su historia aportan de manera minoritaria a la producción de vino del país, pero que se encuentran en crecimiento y revisten de gran interés socioeconómico y cultural. Asimismo, y a pesar del marcado interés regional, no se descarta que dichos resultados pudieran ser extrapolados a regiones con características similares.
Bartowsky , E. (2005). Oenococcus oeni and malolactic fermentation–moving into the molecular arena. ustralian Journal of Grape Wine Research, 11(2), 174-187.
Bartowsky, E. J., & Borneman, A. R. (2011). Genomic variations of Oenococcus oeni strains and the potential to impact on malolactic fermentation and aroma compounds in wine. Applied Microbiology Biotechnology, 92, 441-447.
Berbegal, C., Peña, N., Russo, P., Grieco, F., Pardo, I., et al. (2016). Technological properties of Lactobacillus plantarum strains isolated from grape must fermentation. Food Microbiology, 57, 187-194.
Betteridge, A., Grbin, P., & Jiranek, V. (2015). Improving Oenococcus oeni to overcome challenges of wine malolactic fermentation. Trends in biotechnology, 33(9), 547-553.
Bokulich, N. A., Thorngate, J. H., Richardson, P. M., & Mills, D. A. (2014). Microbial biogeography of wine grapes is conditioned by cultivar, vintage, and climate. Proceedings of the National Academy of Sciences, 111(1), E139-E148.
Borneman, A. R., McCarthy, J. M., Chambers, P. J., & Bartowsky, E. (2012). Comparative analysis of the Oenococcus oeni pan genome reveals genetic diversity in industrially-relevant pathways. BMC genomics, 13, 1-13.
Bravo-Ferrada, B. M., Hollmann, A., Delfederico, L., Valdés La Hens, D., Caballero, A., et al. (2013). Patagonian red wines: selection of Lactobacillus plantarum isolates as potential starter cultures for malolactic fermentation. World Journal of Microbiology Biotechnology, 29, 1537-1549.
Bravo‐Ferrada, B. M., Tymczyszyn, E. E., Gómez‐Zavaglia, A., & Semorile, L. (2014). Effect of acclimation medium on cell viability, membrane integrity and ability to consume malic acid in synthetic wine by oenological Lactobacillus plantarum strains. Journal of applied microbiology, 116(2), 360-367.
Brizuela, N. S., Franco‐Luesma, E., Bravo‐Ferrada, B. M., Pérez‐Jiménez, M., Semorile, L., et al. (2021). Influence of Patagonian Lactiplantibacillus plantarum and Oenococcus oeni strains on sensory perception of Pinot Noir wine after malolactic fermentation. Australian Journal of Grape Wine Research, 27(1), 118-127.
Cabrera. (1976). Regiones fitogeográficas argentinas. nciclopedia argentina de agricultura y jardinería, 2, 1-85.
Campo, A., Ramos, M. B., & Zapperi, P. (2009). Análisis de las variaciones anuales de precipitación en el suroeste bonaerense, Argentina. XII Encuentro de Geógrafos de América Latina, 12.
Campo, A. M., Gil, V., Gentili, J. O., Volonté, A., & Duval, V. (2011). Inventario de eventos climáticos-meteorológicos extremos. Suroeste Bonaerense (1995-2010). Párrafos geográficos, 10(1), 102-115.
Cao, W., Shu, N., Wen, J., Yang, Y., Jin, Y., et al. (2022). Characterization of the key aroma volatile compounds in nine different grape varieties wine by headspace gas chromatography–ion mobility spectrometry (HS-GC-IMS), odor activity values (OAV) and sensory analysis. Foods, 11(18), 2767.
Capozzi, V., Di Toro, M. R., Grieco, F., Michelotti, V., Salma, M., et al. (2016). Viable But Not Culturable (VBNC) state of Brettanomyces bruxellensis in wine: New insights on molecular basis of VBNC behaviour using a transcriptomic approach. Food Microbiology, 59, 196-204.
Capozzi, V., Ladero, V., Beneduce, L., Fernández, M., Alvarez, M. A., et al. (2011). Isolation and characterization of tyramine-producing Enterococcus faecium strains from red wine. Food Microbiology, 28(3), 434-439.
del Carmen Portillo, M., & Mas, A. (2016). Analysis of microbial diversity and dynamics during wine fermentation of Grenache grape variety by high-throughput barcoding sequencing. LWT-Food Science Technology, 72, 317-321.
Delfederico, L., Hollmann, A., Martínez, M., Iglesias, N. G., De Antoni, G., et al. (2006). Molecular identification and typing of lactobacilli isolated from kefir grains. Journal of Dairy Research, 73(1), 20-27.
DeSantis, T. Z., Hugenholtz, P., Larsen, N., Rojas, M., Brodie, E. L., et al. (2006). Greengenes, a chimera-checked 16S rRNA gene database and workbench compatible with ARB. Applied environmental microbiology, 72(7), 5069-5072.
du Toit, M., Engelbrecht, L., Lerm, E., & Krieger-Weber, S. (2011). Lactobacillus: the next generation of malolactic fermentation starter cultures—an overview. Food Bioprocess Technology, 4, 876-906.
Escobar-Zepeda, A., Vera-Ponce de León, A., & Sanchez-Flores, A. (2015). The road to metagenomics: from microbiology to DNA sequencing technologies and bioinformatics. Frontiers in genetics, 6, 155161.
Fichot, E. B., & Norman, R. S. (2013). Microbial phylogenetic profiling with the Pacific Biosciences sequencing platform. Microbiome, 1, 1-5.
Gobert, A., Evers, M. S., Morge, C., Sparrow, C., & Delafont, V. (2022). Comparison of DNA purification methods for high‐throughput sequencing of fungal communities from wine fermentation. MicrobiologyOpen, 11(5), e1321.
Hall, M. E., Cadle-Davidson, L., Fang, Z., & Wilcox, W. F. (2019). A new method for extracting DNA from the grape berry surface, beginning in the vineyard. Heliyon, 5(10).
INV. (2021). Instituto Nacional de Vitivinicultura.
Iorizzo, M., Testa, B., Lombardi, S. J., García-Ruiz, A., Muñoz-González, C., et al. (2016). Selection and technological potential of Lactobacillus plantarum bacteria suitable for wine malolactic fermentation and grape aroma release. Lwt, 73, 557-566.
Işçi, B., Kalkan Yildirim, H., & Altindisli, A. (2014). Evaluation of methods for DNA extraction from must and wine. Journal of the Institute of Brewing, 120(3), 238-243.
Jara, C., Mateo, E., Guillamón, J., Torija, M., & Mas, A. (2008). Analysis of several methods for the extraction of high quality DNA from acetic acid bacteria in wine and vinegar for characterization by PCR-based methods. International journal of food microbiology, 128(2), 336-341.
Jin, G., Jiranek, V., Hayes, A. M., & Grbin, P. R. (2022). Isolation and characterization of high-ethanol-tolerance lactic acid bacteria from Australian Wine. Foods, 11(9), 1231.
Kioroglou, D. (2020). Analysis of microbial populations in wines through NGS methodologies.
Krieger-Weber, S., Heras, J. M., & Suarez, C. (2020). Lactobacillus plantarum, a new biological tool to control malolactic fermentation: A review and an outlook. Beverages, 6(2), 23.
Lerm, E., Engelbrecht, L., & Du Toit, M. (2011). Selection and characterisation of Oenococcus oeni and Lactobacillus plantarum South African wine isolates for use as malolactic fermentation starter cultures. Stellenbosch University.
Liu. (2002). Malolactic fermentation in wine–beyond deacidification. Journal of applied microbiology, 92(4), 589-601.
Liu, D., Zhang, P., Chen, D., & Howell, K. (2019). From the vineyard to the winery: how microbial ecology drives regional distinctiveness of wine. Frontiers in microbiology, 10, 498313.
Lorentzen, M. P., & Lucas, P. M. (2019). Distribution of Oenococcus oeni populations in natural habitats. Applied Microbiology Biotechnology, 103(7), 2937-2945.
Lucio, O., Pardo, I., Krieger-Weber, S., Heras, J. M., & Ferrer, S. (2016). Selection of Lactobacillus strains to induce biological acidification in low acidity wines. Lwt, 73, 334-341.
McDonald, D., Clemente, J. C., Kuczynski, J., Rideout, J. R., Stombaugh, J., et al. (2012). The Biological Observation Matrix (BIOM) format or: how I learned to stop worrying and love the ome-ome. Gigascience, 1(1), 2047-2217X-2041-2047.
McDonald, D., Price, M. N., Goodrich, J., Nawrocki, E. P., DeSantis, T. Z., et al. (2012). An improved Greengenes taxonomy with explicit ranks for ecological and evolutionary analyses of bacteria and archaea. The ISME journal, 6(3), 610-618.
Millet, V., & Lonvaud‐Funel, A. (2000). The viable but non‐culturable state of wine micro‐organisms during storage. Letters in applied microbiology, 30(2), 136-141.
Montgomery, B. L. (2020). Lessons from microbes: what can we learn about equity from unculturable bacteria? Msphere, 5(5), 10.1128/msphere. 01046-01020.
Morgan, H. H., Du Toit, M., & Setati, M. E. (2017). The grapevine and wine microbiome: insights from high-throughput amplicon sequencing. Frontiers in microbiology, 8, 249460.
Ngwenya, M. P., Nkambule, T. P., & Kidane, S. W. (2023). Physicochemical attributes and acceptability of marula wine fermented with natural Lactiplantibacillus plantarum and Saccharomyces cerevisiae. Heliyon, 9(11).
OIV. (2021). Organización Internacional de la Viña y el Vino - State of the world vitivinicultural sector in 2019.
Ospital, M. S. (2003). Vino en la pampa: La actividad vitivinícola en la provincia de Buenos Aires, 1900-1940. Mundo agrario.
Ospital, M. S. (2019). Políticas reguladoras en la vitivinicultura argentina. Crisis e intervención del Estado. 1930-1940. Encuentros Latinoamericanos, 3(1), 95-116.
Oyuela Aguilar, M., Gobbi, A., Browne, P. D., Ellegaard-Jensen, L., Hansen, L. H., et al. (2020). Influence of vintage, geographic location and cultivar on the structure of microbial communities associated with the grapevine rhizosphere in vineyards of San Juan Province, Argentina. PLoS One, 15(12), e0243848.
Paolinelli, M., Martinez, L. E., Garcia Lampasona, S. C., Diaz Quirós, C., Belmonte, M., et al. (2023). Microbiome in soils of Mendoza: microbial resources for the development of agroecological management in viticulture.
Pérez-Martín, F., Seseña, S., Izquierdo, P. M., & Palop, M. L. (2014). Are Enterococcus populations present during malolactic fermentation of red wine safe? Food Microbiology, 42, 95-101.
Pinto, C., Pinho, D., Cardoso, R., Custódio, V., Fernandes, J., et al. (2015). Wine fermentation microbiome: a landscape from different Portuguese wine appellations. Frontiers in microbiology, 6, 132363.
Pinto, C., Pinho, D., Sousa, S., Pinheiro, M., Egas, C., et al. (2014). Unravelling the diversity of grapevine microbiome. PLoS One, 9(1), e85622.
Rivas, G. A., Guillade, A. C., Semorile, L. C., & Delfederico, L. (2021). Influence of climate on soil and wine bacterial diversity on a vineyard in a non-traditional wine region in Argentina. Frontiers in microbiology, 12, 726384.
Rivas, G. A., Semorile, L., & Delfederico, L. (2022). Microbial diversity of the soil, rhizosphere and wine from an emerging wine-producing region of Argentina. Lwt, 153, 112429.
Rodas, A. M., Ferrer, S., & Pardo, I. (2003). 16S-ARDRA, a tool for identification of lactic acid bacteria isolated from grape must and wine. Systematic Applied Microbiology, 26(3), 412-422.
Spano, G., Russo, P., Lonvaud-Funel, A., Lucas, P., Alexandre, H., et al. (2010). Biogenic amines in fermented foods. European journal of clinical nutrition, 64(3), S95-S100.
Stenlid, J., Karlsson, J.-O., & Högberg, N. (1994). Intraspecific genetic variation in Heterobasidion annosum revealed by amplification of minisatellite DNA. Mycological research, 98(1), 57-63.
Stewart, E. J. (2012). Growing unculturable bacteria. Journal of bacteriology, 194(16), 4151-4160.
Swiegers, J. H., & Pretorius, I. S. (2005). Yeast modulation of wine flavor. Advances in applied microbiology, 57, 131-175.
Takahashi, M., Kita, Y., Mizuno, A., & Goto-Yamamoto, N. (2017). Evaluation of method bias for determining bacterial populations in bacterial community analyses. Journal of bioscience bioengineering, 124(4), 476-486.
Tedesco, F., Siesto, G., Pietrafesa, R., Romano, P., Salvia, R., et al. (2022). Chemical methods for microbiological control of winemaking: An overview of current and future applications. Beverages, 8(3), 58.
Vega-Avila, A. D., Gumiere, T., Andrade, P. A. M., Lima-Perim, J., Durrer, A., et al. (2015). Bacterial communities in the rhizosphere of Vitis vinifera L. cultivated under distinct agricultural practices in Argentina. Antonie Van Leeuwenhoek, 107, 575-588.
Virdis, C., Sumby, K., Bartowsky, E., & Jiranek, V. (2021). Lactic acid bacteria in wine: Technological advances and evaluation of their functional role. Frontiers in microbiology, 11, 612118.
Williams, J. G., Kubelik, A. R., Livak, K. J., Rafalski, J. A., & Tingey, S. V. (1990). DNA polymorphisms amplified by arbitrary primers are useful as genetic markers. Nucleic acids research, 18(22), 6531-6535.
Xu, Z., Lu, Z., Soteyome, T., Ye, Y., Huang, T., et al. (2021). Polymicrobial interaction between Lactobacillus and Saccharomyces cerevisiae: coexistence-relevant mechanisms. Critical Reviews in Microbiology, 47(3), 386-396.

