Producción pública de biofármacos en Argentina
Public production of biopharmaceuticals in Argentina
Noelia BurgardtLa Producción Pública de Medicamentos (PPM) surge en Argentina como una estrategia para el abastecimiento de insumos sanitarios estratégicos (Zelaya et al. 2021). Durante los vaivenes en la historia de nuestro país la PPM ha logrado mantenerse vigente a pesar de los diversos desafíos políticos y económicos. El vínculo entre la PPM y las necesidades sanitarias fue evidente desde sus inicios. El primer laboratorio fue creado como consecuencia de las políticas implementadas frente a los brotes de cólera de 1867 y 1871. En primer lugar fue creada una sección bacteriológica dentro del Departamento Nacional de Higiene en 1880 liderada por el Dr. Carlos Malbrán. Luego durante el gobierno de Yrigoyen esta sección fue convertida en el Instituto Bacteriológico en 1916 el primer laboratorio público encargado de producir medicamentos para enfermedades infectocontagiosas.
La Secretaría de Salud de la Nación a cargo del Dr. Ramón Carrillo fue creada durante el primer gobierno de Juan Domingo Perón. Ese mismo año en 1946 fue creada la empresa Especialidades Medicinales del Estado aprovechando las instalaciones de los laboratorios alemanes apropiados en el contexto de la Segunda Guerra Mundial. La importancia que daba este gobierno a las políticas sanitarias fue puesta en evidencia con la creación del Ministerio de Salud de la Nación en 1949. Poco después en 1950 fue inaugurado el “Instituto Biológico” perteneciente al Ministerio de Salud de la Provincia de Buenos Aires. Con el objetivo de proporcionar medicamentos de calidad a la población estos laboratorios públicos contribuyeron a la regulación de precios y el control del mercado de medicamentos considerados de primera necesidad. Las empresas que conformaban Especialidades Medicinales del Estado fueron restituidas a manos privadas durante la dictadura cívico-militar que gobernó a partir de 1955 tras derrocar a Perón. La llegada al país de grandes empresas farmacéuticas multinacionales y la liberación de los precios de los medicamentos fueron impulsadas por la Ley de Inversiones Extranjeras en 1958 promulgada durante esta dictadura.
Más adelante durante el gobierno de Illia surgieron nuevamente políticas vinculadas con el sector farmacéutico. Las Leyes Oñativia de 1964 fueron sancionadas con la intención de controlar la comercialización de medicamentos para contrarrestar la extranjerización del mercado. Además fue creada la Planta de Proteínas Plasmáticas en 1963 predecesora del Laboratorio de Hemoderivados de la Universidad Nacional de Córdoba. Las leyes Oñativia fueron derogadas en el gobierno de facto de Onganía favoreciendo nuevamente la desregulación y concentración de la industria farmacéutica en Argentina.
Hubo un breve retorno a políticas sanitarias sociales durante el gobierno de Alfonsín cuando fue creado el Fondo de Asistencia en Medicamentos en 1984 destinado a brindar medicamentos gratuitos a los grupos desprotegidos. Entre 1989-2001 fueron nuevamente aplicadas medidas para favorecer la apertura económica la desregulación y la concentración del mercado farmacéutico durante los gobiernos de Menem y de la Rúa. La Administración Nacional de Medicamentos Alimentos y Tecnología Médica (ANMAT) fue creada en 1992 para asegurar la calidad de la producción farmacéutica. Luego en 1996 fue promulgada la Ley de Patentes de Invención la cual impactó en el crecimiento de empresas extranjeras en el sector. También en 1996 fue creada la Administración Nacional de Laboratorios e Institutos de Salud “Dr. Carlos Malbrán” (ANLIS) como un organismo público descentralizado dependiente del Ministerio de Salud de la Nación Argentina (MINSal). Paradójicamente muchos laboratorios públicos se formaron durante estos años como respuesta a las dificultades en el acceso a los medicamentos entre ellos el Laboratorio Farmacéutico Conjunto de las Fuerzas Armadas.
La declaración de la Emergencia Sanitaria Nacional en 2002 en medio de una fuerte crisis política económica y social tuvo como objetivo primordial asegurar la continuidad de los servicios de salud y el acceso a los medicamentos. Esta medida se sostuvo durante el gobierno de Kirchner aunque la PPM no fue inicialmente considerada como instrumento político. Mientras tanto por fuera del ámbito gubernamental una serie de actividades de apoyo a la PPM fueron impulsadas por actores del sector universitario y científico-tecnológico llevando a la creación de la Multisectorial por la Producción Pública de Medicamentos y Vacunas en 2005. Fue recién en 2008 durante el primer gobierno de Cristina Fernández de Kirchner que la PPM fue incorporada por primera vez como una política estratégica creando el Programa Nacional para la Producción Pública de Medicamentos Vacunas y Productos Médicos en el MINSal. Esta medida fue consolidada como política pública en 2011 mediante la sanción de la Ley N° 26.688 que declara de interés nacional la investigación y producción pública de medicamentos.
Durante estos años también se fueron implementando medidas que llevaron a la incorporación de la PPM en la agenda de Ciencia Tecnología e Innovación (CTI). Si bien los laboratorios públicos ya formaban parte del complejo científico-tecnológico argentino no se contaba con instrumentos de financiación específicos para este sector. El proceso de consolidación de la PPM como parte de las políticas públicas coincidió con la aplicación de una serie de medidas de jerarquización de la CTI (Burgardt González Maglio y Piñero 2021). La creación del Fondo Argentino Sectorial (FONARSEC) en 2009 y de los Fondos de Innovación Tecnológica Sectorial (FITS) fueron clave en ese proceso ya que buscaron vincular al sector científico con las demandas de distintos sectores productivos. La PPM fue incorporada como sector prioritario en 2011 dando como resultado la convocatoria FITS-Salud PPM en 2013. Así fueron financiados 5 proyectos de I+D fortaleciendo el trabajo conjunto entre instituciones de CTI y de PPM para la innovación y el desarrollo de medicamentos estratégicos. Las líneas de investigación y desarrollo enfocadas en PPM buscaron resolver problemáticas propias de nuestro país generando capacidades en diversas áreas tecnológicas y contribuyendo en la construcción de soberanía tanto en salud como en CTI.
La Agencia Nacional de Laboratorios Públicos (ANLAP) fue creada por Ley N° 27.113 en 2015 durante el segundo gobierno de Cristina Fernández de Kirchner. Su votación fue aprobada con sólo cuatro abstenciones en Diputados y por unanimidad en Senadores. En el comienzo del gobierno de Mauricio Macri muchas dependencias del Estado fueron paralizadas llevando a que la ANLAP recién pueda alcanzar su funcionamiento operativo en 2017 (Isturiz Díaz de Guijarro y Naidorf 2018). A fines de 2019 la estructura de laboratorios de la Agencia estaba conformada por 34 instituciones las cuales contaban con la capacidad para fabricar gran parte de los medicamentos que la Organización Mundial de la Salud (OMS) definió como esenciales (ANLAP 2019). A partir de 2020 en el gobierno de Fernández la gestión de la Agencia fue enmarcada dentro de una Política Nacional de Medicamentos con el objetivo de articular promover y fortalecer la investigación desarrollo y producción pública de medicamentos y otras tecnologías sanitarias para promover su acceso a lo largo del territorio nacional (ANLAP 2023). El rol de ANLAP fue clave en el diseño de la convocatoria del FONARSEC “Proyectos Estratégicos - Producción Pública de Medicamentos 2021” (PE-PPM 2021) y demostró una mejor comprensión del sector (Agencia Nacional de Promoción de la Investigación el Desarrollo Tecnológico y la Innovación 2021). Las tres líneas estratégicas fueron definidas en articulación entre ANLAP el Ministerio de Ciencia Tecnología e Innovación (MINCyT) y la Agencia Nacional de Promoción de la Investigación el Desarrollo Tecnológico y la Innovación (I+D+i). Como resultado fueron aprobados 19 proyectos de investigación y desarrollo (I+D) pertenecientes a 9 jurisdicciones del país. Además fruto del trabajo de la ANLAP durante 2020-2023 fueron lanzados nuevos productos como Fierritas Carbatest Misoprostol y Mifepristona. Un gran número de proyectos de investigación desarrollo y modernización tecnológica fueron financiados por fondos propios de la agencia mediante concursos abiertos a las instituciones adheridas. También fueron elaborados por la ANLAP informes sobre temas vinculados a la producción de principios activos y a la producción de vacunas del calendario nacional (ANLAP 2023). La I+D en medicamentos fue también impulsada por ANLAP mediante la creación de becas cofinanciadas con CONICET las cuales fueron otorgadas para la realización de doctorados y posdoctorados en temas estratégicos. El trabajo coordinado entre los laboratorios estatales y la ANLAP entre 2019-2023 fue crucial para que el Estado pueda establecer precios testigos garantizar el acceso a medicamentos estratégicos y financiar proyectos de investigación y desarrollo enfocados en las necesidades sanitarias de nuestro país.
Recientemente la ANLAP fue suprimida a través del Decreto Nacional de Urgencia 70/2023 (DNU) por decisión unilateral del poder ejecutivo apenas iniciado el gobierno de Milei. Así en apenas un mes del inicio del gobierno se perdieron los recursos humanos que formaban parte de la ANLAP los fondos para el financiamiento de proyectos estratégicos de salud pública y la capacidad de coordinación entre los laboratorios públicos. Este DNU puso en riesgo muchos de los avances logrados en cuanto a la producción pública de medicamentos y además atenta contra la salud de la gente al modificar legislación vinculada con la dispensa de medicamentos. A pocos tiempo de su aplicación el impacto negativo de estas medidas ya se refleja en una disminución en el acceso a los medicamentos (Gollán 2024). Frente a esto los laboratorios públicos enfrentan nuevamente el desafío de sostener la PPM como un instrumento político que contribuya a garantizar el acceso a los medicamentos.
A partir de la revisión de la historia de la PPM podemos ver que hubo diferentes gobiernos que tomaron medidas y políticas públicas para impulsar su crecimiento. La falta de apoyo político sostenido en el tiempo es una de las mayores dificultades que encontró este sector para alcanzar su máxima capacidad. Sin embargo incluso en períodos donde no se dieron condiciones favorables la PPM logró sostener su rol como proveedor de medicamentos. Por supuesto que los mayores avances del sector se observan en la etapa donde fueron consolidadas políticas públicas sobre medicamentos ciencia tecnología e innovación entre 2011-2015 y 2019-2023. En este trabajo nos interesa enfocar el análisis en la producción pública de biofármacos. Nos preguntamos si estas políticas han logrado un impacto positivo en las capacidades tecnológicas de los laboratorios públicos que producen medicamentos biológicos. Para responder esto planteamos como objetivo recopilar y analizar las capacidades públicas de investigación desarrollo y producción de biofármacos atendiendo las siguientes dimensiones: capacidades productivas actuales habilitaciones de plantas proyectos de I+D en curso tipo de productos biológicos elaborados tecnologías productivas y capacidades potenciales.
Como metodología para obtener datos sobre las dimensiones propuestas realizamos una revisión de fuentes de información primarias y secundarias. Para el caso de las fuentes primarias la técnica utilizada de producción y recolección de la información fue la entrevista mediante la implementación de un guión semi estructurado. Las entrevistas fueron realizadas al director/a técnico/a de la institución o al responsable designado/a por esa autoridad. Debido al contexto de pandemia de COVID-19 algunas de las entrevistas fueron realizadas por videollamada y en otros casos fueron realizadas durante visitas en la institución correspondiente. Las fuentes de información secundarias que fueron consultadas y analizadas involucraron bibliografía específica sobre la temática investigaciones académicas datos proporcionados por la ANLAP datos estadísticos documentos oficiales y normativa específica.
En nuestro país hay cinco laboratorios públicos que producen biofármacos (Tabla 1) los cuales fueron creados en diferentes épocas de nuestra historia (Figura 1). Estos laboratorios cuentan con infraestructura y equipamiento de alto nivel con excelentes profesionales y con sus correspondientes habilitaciones (Burgardt 2022).
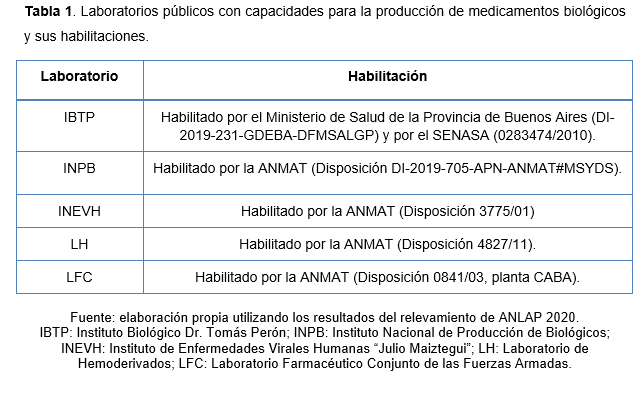

El Instituto Biológico Dr. Tomás Perón (IBTP) tiene habilitación del Ministerio de Salud de la Provincia de Buenos Aires (PBA) como productor de biológicos y del Servicio Nacional de Sanidad y Calidad Agroalimentaria (SENASA) para producir vacunas virales (Tabla 1). Este organismo pertenece a la Subsecretaría de Planificación y Control Sanitario y ejecuta las políticas del Ministerio de Salud de la PBA en lo que respecta a servicios de calidad en el diagnóstico de enfermedades infectocontagiosas, producción de medicamentos y productos biológicos, control de calidad, inscripción y reinscripción de medicamentos y productos farmacéuticos, ensayos fisicoquímicos y microbiológicos, y poder de policía vinculado a productos industriales, cosméticos, sanitarios y materiales en contacto con alimentos. La historia del IBTP comienza luego de la creación del Ministerio de Salud de la PBA en el año 1947 cuando el entonces Instituto de Investigaciones Patológicas e Higiénicas cambia de dependencia y pasa a ser renombrado como “Instituto Biológico”. Unos años después, en 1949, fue iniciada la construcción de su edificio, el cual fue inaugurado por Eva Perón en 1950 (Instituto Biológico Dr. Tomás Perón 2019). Desde entonces, el instituto produce los medicamentos que demandan los hospitales públicos de la Provincia. En cuanto a la producción de biofármacos, el IBTP cuenta con una planta de vacunas y sueros y una planta de vacunas virales, entre las que se producen sueros, antitoxinas, vacunas bacterianas, vacunas virales, alérgenos e inmunomoduladores (Centeno 2016). Durante muchos años ha logrado abastecer al Ministerio de Salud de la PBA con BCG, BCG Inmunoterapéutica, Doble Bacteriana y Antirrábica. Actualmente, la mayor parte de estas vacunas se dejaron de producir debido a los cambios en las recomendaciones de seguridad en la producción y a la modificación de la demanda del sistema sanitario (Corvalán 2017). Sin embargo, el instituto conserva capacidades para la elaboración de estos productos y lleva adelante proyectos de investigación y desarrollo en conjunto con la Comisión de Investigaciones Científicas de la PBA, la Universidad de La Plata e institutos del Consejo Nacional de Investigaciones Científicas y Técnicas (CONICET). En 2023 se realizó la presentación a la Legislatura de PBA de un proyecto de ley para la creación de un “Centro de Industria Farmacéutica Bonaerense” el cuál funcionará dentro del IBTP (Lavecchia 2023). La iniciativa contempla una inversión para la construcción y equipamiento de un nuevo polo productivo, científico y tecnológico que reactive la producción pública de medicamentos y vacunas y el control de calidad de alimentos, envases y fármacos.
El Instituto Nacional de Producción de Biológicos (INPB) pertenece a la ANLIS y cuenta con habilitación de ANMAT como establecimiento elaborador, importador y exportador de medicamentos de origen biológico (Tabla 1). Este laboratorio fue creado como instituto en 1996 junto con la creación de la ANLIS. En sus comienzos, se encargaba de la producción de una gran cantidad de biofármacos, pero a finales de los años 90 se dejaron de producir muchos de ellos (Corvalán 2017). A pesar de esto, se mantuvo la capacitación del personal y se llevaron adelante diversos proyectos de I+D en colaboración con otros países, permitiendo que el laboratorio retome la planificación de la producción de estos biofármacos. Actualmente se están llevando adelante proyectos para la producción de vacunas y se encuentran en construcción 3 plantas para la producción industrial de vacunas, financiados por ANLIS y por subsidios del FONARSEC. Una de las instalaciones será para la producción de vacuna antirrábica, otra será para la producción BCG y la tercera planta será para vacunas bacterianas, toxinas y recombinantes (Pérez Ponsa et al. 2023).
El Instituto Nacional de Enfermedades Virales Humanas (INEVH) fue creado en 1978 y también pertenece a la ANLIS. El laboratorio cuenta con capacidades tecnológicas para producir vacunas virales, siendo su producto actual la vacuna Candid #1 contra la Fiebre Hemorrágica Argentina (Ambrosio et al. 2006). El INEVH también produce plasma inmune para el tratamiento de la Fiebre Hemorrágica Argentina y reactivos para diagnóstico de referencia de Arenavirus, Hantavirus, Dengue, Fiebre Amarilla y otras Arbovirosis. La planta fue habilitada en 2001 por la ANMAT para la producción de vacunas de virus vivos atenuados para uso humano (Tabla 1). Las instalaciones cuentan con un bioterio, un laboratorio de cultivos celulares certificados, un laboratorio de control de calidad y una sección de producción de vacunas. Los tres últimos sectores cuentan con sistemas de manejo del aire y circulación controlada de insumos, personas y residuos correspondientes al nivel III de bioseguridad. En 2020 se inició una inversión para la readecuación de la planta de producción, una nueva planta de agua, remodelación de edificios y del laboratorio de virología, mejoras de los laboratorios de bioseguridad y restauración del sector de obtención de plasma. Recientemente fueron adjudicados fondos para ampliar las instalaciones y las capacidades del INEVH para la construcción de una nueva planta de producción de 720 m2 (Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación [I+D+i] 2022). Estos fondos incluyen la ejecución de la obra y la adquisición de equipamiento como equipos de laboratorio, sistema de purificación de agua de calidad farmacéutica, validador térmico y estufas para la producción de vacunas, recambio y actualización de equipos de cámara fría, mobiliario y mantenimiento. La ampliación de la planta productora va a incorporar nuevos laboratorios y refuncionalizar parte de otros existentes, permitiendo llevar la producción de Candid #1 a su capacidad máxima e incorporar nuevas prestaciones para la producción de sustancias bioquímicamente activas mediante cultivo de células.
El Laboratorio de Hemoderivados (LH) pertenece a la Universidad Nacional de Córdoba y cuenta con habilitación nacional de ANMAT para la elaboración, importación y exportación de especialidades medicinales derivadas del plasma humano (Tabla 1). Esa institución elabora medicamentos como albúmina, inmunoglobulinas y gammaglobulinas, antitrombina III, factor VIII, entre otros. Fue creado en 1963, poniendo en marcha el primer fraccionamiento de plasma humano en 1972 y logrando la habilitación del primer lote oficial de albúmina en 1974 (Massa 2013). Poco después, el laboratorio también producía y comercializaba gammaglobulina poliespecífica intramuscular. A lo largo del tiempo, esta empresa universitaria logró crecer y diversificarse, incorporando la producción de inyectables de bajo volumen, medicamentos genéricos, productos óseos y soluciones para conservación de órganos. Gracias al plan integral de expansión y actualización tecnológica aplicado entre 2010-2016, sus plantas se duplicaron en superficie y se automatizaron procesos, logrando que se duplique la capacidad productiva de hemoderivados y que se quintuplique la producción de medicamentos genéricos inyectables. Durante este período, también se fortaleció el vínculo con grupos de investigación y desarrollo de la Universidad Nacional de Córdoba y del CONICET a través de diversos proyectos de investigación y desarrollo. Las dos plantas de producción de proteínas plasmáticas cumplen con exigencias de Buenas Prácticas de Fabricación similares a las requeridas para la producción de medicamentos biotecnológicos. Las mismas tienen en conjunto un sector de fraccionamiento plasmático, otro sector de purificación o elaboración, una sala de envasado aséptico con liofilizador y salas de almacenamiento a bajas temperaturas. Actualmente, este laboratorio es un complejo industrial importante y moderno que le permite a Argentina y a cuatro países de la región disponer de medicamentos estratégicos.
El Laboratorio Farmacéutico Conjunto de las Fuerzas Armadas (LFC) fue creado en el año 2000 y depende del Estado Mayor Conjunto. Tiene como objetivo proveer de medicamentos estratégicos a las Fuerzas Armadas y organismos oficiales. Cuenta con dos establecimientos (Planta Caseros y Planta Palomar) donde se elaboran y analizan medicamentos, productos biológicos y antibióticos. Esta institución cuenta con un área de envasado de inyectables con capacidades tecnológicas para producir antivenenos y para formular vacunas. Recientemente fueron realizadas obras en sus instalaciones, las cuales fueron financiadas por el Ministerio de Defensa (Ministerio de Defensa 2021). Se modernizó la sección de líquidos de la Planta de Caseros con la adquisición de un reactor de 500 litros y una llenadora donde se produce alcohol en gel y repelente para mosquitos DEET y se colocaron extractores de aire con una tecnología que evita la propagación de bacterias y virus a través del aire.
Estos laboratorios públicos, con excepción del LFC, manejan diversas tecnologías para el cultivo de células. Este tipo de tecnologías pueden ser aplicadas en la producción de distintos tipos de biofármacos (Tabla 2). En algunos casos, estas tecnologías son parte actualmente de procesos de producción de biológicos, mientras que en otros casos se encuentran en desarrollo para la producción de nuevos productos biológicos.

Los medicamentos biológicos son indispensables para el tratamiento de diversos tipos de enfermedades. La mayoría de los biofármacos usados como ingredientes farmacéuticos activos son proteínas como por ejemplo hormonas, inmunoglobulinas y anticuerpos. Según ANMAT, los medicamentos de origen biológico son aquellos productos obtenidos a partir de organismos vivos o de sus tejidos (Sánchez 2020). Estos incluyen a los virus, sueros terapéuticos, toxinas, antitoxinas, vacunas, sangre, componentes o derivados de la sangre, productos alergénicos, hormonas, factores estimulantes de colonias, citoquinas, anticuerpos, heparinas, entre otros. Estos productos son utilizados para fines de la prevención, del tratamiento o del diagnóstico de ciertas enfermedades.
Los biofármacos pueden ser obtenidos mediante procesos extractivos (usando fuentes naturales de origen humano o animal) o por técnicas biotecnológicas basadas en cultivo de células y/o ingeniería genética (OMS 1991). Los procesos biotecnológicos permiten obtener mayores rendimientos que los métodos extractivos. Además, los productos obtenidos de esta forma presentan menores chances de generar efectos adversos en relación a los obtenidos de fuentes naturales. La primera generación de productos farmacéuticos biotecnológicos fue lanzada en la década de 1980. Estos consisten en macromoléculas de complejidad baja-media, es decir, proteínas de bajo peso molecular con estructura y complejidad molecular relativamente baja. Algunos ejemplos son las epoetinas, los factores estimulantes de la médula ósea, las somatotropinas y la insulina. En el caso de las vacunas, las técnicas biotecnológicas han permitido que sean perfeccionados los procesos de producción y de control de calidad, así como también el desarrollo de nuevas tecnologías. Las vacunas tradicionales se obtienen a partir de virus, bacterias o toxinas atenuadas o inactivadas, mientras que las vacunas biotecnológicas pueden ser basadas en proteínas o en ácidos nucleicos. Con el avance de la biotecnología moderna se desarrollaron proteínas terapéuticas de alta complejidad, dando lugar a la segunda generación de medicamentos biotecnológicos. En este caso, son macromoléculas de peso molecular, estructura y complejidad molecular alta, como anticuerpos monoclonales (mAbs), proteínas de fusión y oligonucleótidos. Los vencimientos de patentes han dado lugar al desarrollo de sustitutos "genéricos" de los productos biotecnológicos originales, denominados biosimilares (Matar 2017). Los medicamentos biosimilares deben demostrar ser similares a un bioterapéutico innovador mediante estudios analíticos, preclínicos y clínicos comparativos. El negocio de los biosimilares en Latinoamérica está en pleno desarrollo y avanza a paso firme en la región (Ortiz-Prado et al. 2020).
En Argentina, la industria de medicamentos biotecnológicos surgió con la creación de la empresa Biosidus en 1983 (Aguiar Fressoli y Thomas 2007). La investigación, desarrollo y producción de biofármacos ha sido impulsada por diversas políticas públicas, muchas de ellas enmarcadas en el plan de Ciencia y Tecnología Argentina Innovadora 2020 (Ministerio de Ciencia, Tecnología e Innovación Productiva 2012). Esto llevó a un aumento de la producción de biosimilares en laboratorios nacionales y a la construcción de la primera fábrica de anticuerpos monoclonales biosimilares de Sudamérica en 2012.
Los laboratorios estatales producen biofármacos que son considerados estratégicos para el sistema de salud. Uno de los motivos más usuales para que un medicamento sea clasificado como estratégico es la ausencia de comercialización por parte de laboratorios privados, debido a que la baja rentabilidad de los mismos los hacen poco atractivos para su elaboración. Luego de la experiencia adquirida en la pandemia de COVID-19, quedó en evidencia la importancia de contar con las capacidades locales para producir medicamentos esenciales, como por ejemplo vacunas recombinantes (Gutman, Lavarello y Pita 2020).
La caracterización de la demanda del sector sanitario es el primer paso para poder contar con datos actualizados sobre los medicamentos estratégicos. En esa línea, la ANLAP realizó un relevamiento de los medicamentos adquiridos por los programas de salud del MINSal durante 2020-2021 (Burgardt 2022). Algunos de los medicamentos del relevamiento fueron identificados como estratégicos ya que se detectaron dificultades para su adquisición, quedaron vacantes en licitaciones y/o estuvieron relacionados con necesidades no satisfechas. Entre los biofármacos definidos como estratégicos en este relevamiento encontramos anticuerpos monoclonales, oligonucleótidos, péptidos y proteínas. El anticuerpo monoclonal Pembrolizumab, considerado como estratégico en este análisis, está listado entre las 10 primeras tecnologías priorizadas del informe de CONETEC (CONETEC 2021) y en la lista jerarquizada por el MINSal (Gutman, Lavarello y Pita 2021). En el caso de las vacunas, la comparación entre la demanda y las capacidades actuales y proyectadas de los laboratorios públicos nos permitió definir un grupo de vacunas del calendario de vacunación nacional que son de alto interés para la producción estatal (Pérez Ponsa et al. 2023).
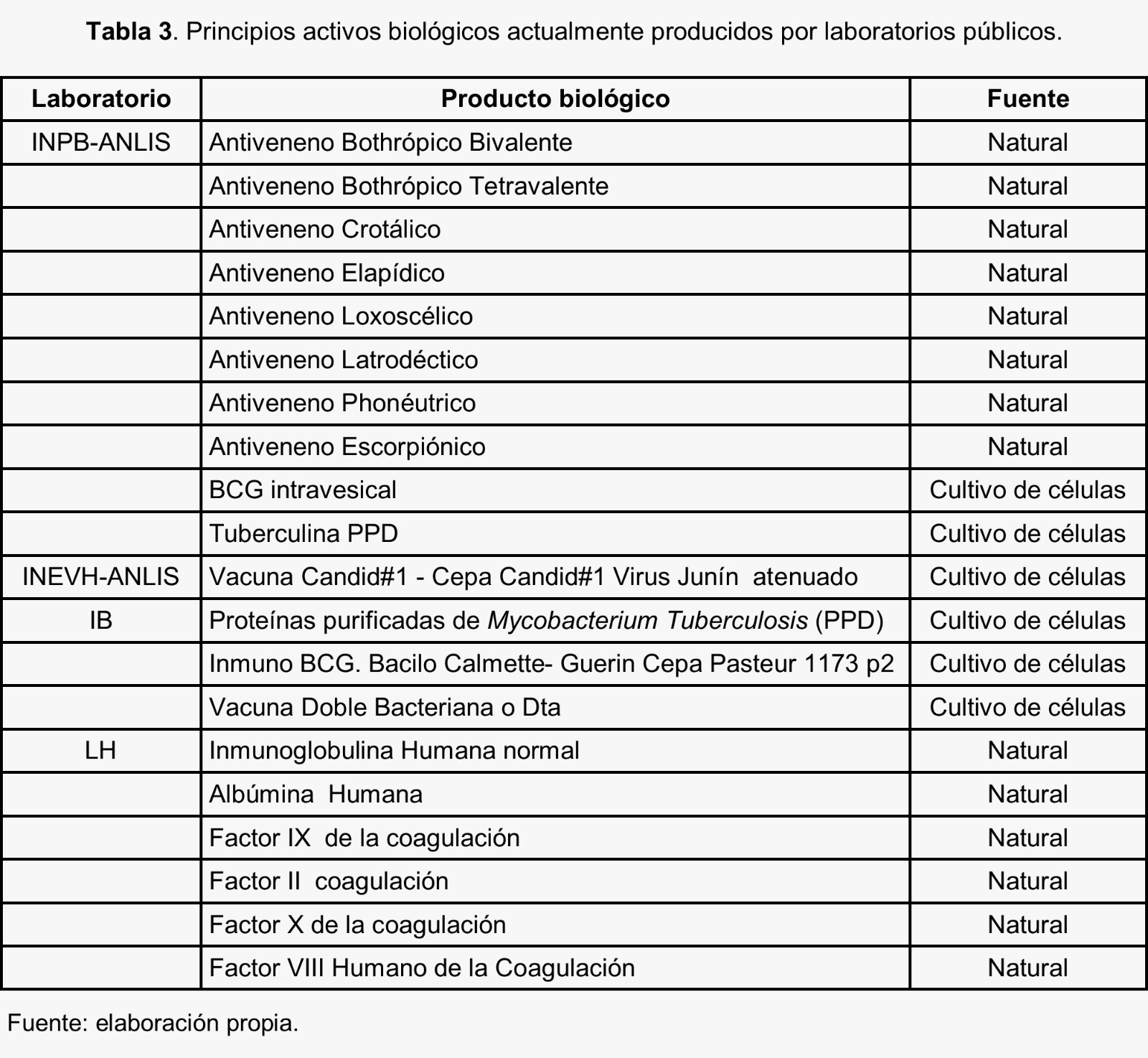
Muchos de los productos biológicos elaborados actualmente por los laboratorios públicos se obtienen a partir del procesamiento de fuentes naturales como por ejemplo suero de plasma humano o suero equino [Espacio para Figura 2] [Espacio para Tabla 3]. Otros son elaborados utilizando tecnología de cultivo de células y/o virus, como es el caso de la BCG intravesical y las vacunas virales.

4.1 Sueros terapéuticos
La terapia con sueros se utiliza desde el siglo 19 para tratar enfermedades infecciosas como la escarlatina (Montelongo-Jauregui et al. 2020). Los sueros hiperinmunes se obtienen a partir del plasma de animales inoculados con toxinas o de pacientes convalecientes. En sus comienzos, el principio activo de los sueros era una mezcla de proteínas plasmáticas sin los factores de coagulación, siendo denominados antisueros de primera generación (García et al. 2011). Este tipo de producto causaba reacciones adversas debido a que algunas proteínas del suero son muy inmunogénicas y potencialmente alergénicas. Fue así que se desarrollaron y aplicaron métodos para purificar las inmunoglobulinas, obteniéndose entonces los sueros de segunda generación. Estos nuevos sueros lograron reducir las reacciones adversas, pero las inmunoglobulinas tienen regiones que producen una activación del sistema inmune y, por lo tanto, dan reacciones similares a la anafilaxia. Además, persistía el problema denominado como la “enfermedad del suero” asociado a los casos donde las personas eran tratadas con sueros antiveneno en más de una ocasión. Esta enfermedad se debe a que los pacientes tratados con sueros de inmunoglobulinas enteras generan una respuesta inmune, produciendo anticuerpos contra el antiveneno o la antitoxina. Por este motivo fueron desarrollados los antisueros de tercera generación, los cuales se obtienen aplicando tratamientos enzimáticos o químicos que eliminan partes de las inmunoglobulinas. Estos antisueros contienen entonces solamente la fracción F(ab´)2 o la fracción Fab de las inmunoglobulinas, disminuyendo la inmunogenicidad y la posibilidad de reacciones adversas.
Las aplicaciones más comunes de los antisueros son como antitoxina, como antiveneno, como tratamiento de algunas enfermedades infecciosas o como reactivos para ensayos de diagnóstico. Los primeros sueros antitoxinas fueron desarrollados en 1890 para el tratamiento de la difteria y del tétanos. A lo largo de la historia se utilizaron sueros terapéuticos para numerosas enfermedades, siendo incluso ensayado como tratamiento en la última pandemia de COVID-19 (Montelongo-Jauregui et al., 2020). En cuanto a los antivenenos, el primer suero fue desarrollado contra veneno de serpiente en 1894 (García el at. , 2011). Los envenenamientos por mordeduras y picaduras de animales ponzoñosos constituyen un serio problema de salud pública en Latinoamérica, afectando mayormente a población vulnerable (Fan et al., 2019). En varios países de la región hay laboratorios productores de antivenenos tanto en el ámbito público como privado. La mayor parte de los antivenenos terapéuticos existentes en el mercado mundial son producidos en equinos. Los antivenenos pueden clasificarse en monovalentes, cuando son eficaces contra una sola especie de veneno, o polivalentes, cuando son eficaces contra varias especies diferentes.
En Argentina se producen antisueros desde la creación del Instituto Bacteriológico en 1916. El Instituto Nacional de Producción de Biológicos produce la mayor cantidad de los antivenenos del país. Su portafolio de productos incluye antivenenos generados contra venenos de serpientes, arañas y escorpiones, los cuales se usan casi exclusivamente en la República Argentina (García el at., 2011). El Instituto cuenta con un serpentario que tiene ejemplares de diferentes latitudes del país y con un campo de inmunizaciones. El procedimiento de producción de suero antiofídico consiste en extraer el veneno de la serpiente, procesarlo e inocular equinos en pequeñas y sucesivas cantidades no letales durante varios meses. En ese período, el caballo genera anticuerpos específicos que son capaces de bloquear las toxinas y que, luego de ser extraídos y procesados, se convierten en el componente principal del antiveneno. El Laboratorio Farmacéutico Conjunto de las Fuerzas Armadas cuenta con la capacidad de producir antivenenos, como el suero antiofídico bivalente, utilizado para contrarrestar mordeduras de yarará y de serpientes cascabel. Utilizan como inóculo venenos donados por ANLIS y cuentan con una instalación del Comando de Remonta y Veterinaria en Campo de Mayo donde realizan la inmunización de los equinos. El suero antiofídico es obtenido del plasma extraído de estos animales, procesado y liofilizado para facilitar su transporte y almacenamiento. El Instituto Biológico Dr. Tomás Perón cuenta con capacidades para producir antisueros, como el suero antilatrodectus (anti viuda negra), el suero antiloxosceles (anti araña de los rincones) y el suero antibotrópico (anti yarará). Además, este laboratorio también cuenta con capacidades para la producción pública de suero antibotulínico y suero antidiftérico (Centeno, 2016; Corvalán, 2017). Finalmente, el INEVH está actualmente encargado de la producción de plasma hiperinmune, que se usa hace décadas para el tratamiento de la Fiebre Hemorrágica Argentina (Ambrosio et al., 2006).
4.2 Vacunas bacterianas y derivados de bacterias
La tuberculosis es producida por el bacilo Mycobacterium tuberculosis y afecta a más de diez millones de personas en todo el mundo. Para la prevención de esta enfermedad se cuenta con una única vacuna antituberculosa, la BCG, la cual ya cumplió 100 años de uso. Esta se obtiene a partir de cultivos de una cepa atenuada de Mycobacterium bovis, denominada Bacilos de Calmette Guérin. La BCG llegó a la Argentina en 1925, gracias a un viaje realizado por el Director del Laboratorio antirrábico del Instituto Bacteriológico de La Plata, el Dr. Andrés Arena, financiado por el gobierno provincial. En el Instituto Pasteur de París Albert Calmette le entregó cultivos de BCG con la condición “que la vacuna debía otorgarse gratuitamente y los cultivos debían facilitarse para quienes los solicitaran para realizar experiencias o investigaciones”. Así, en 1925, el Instituto Bacteriológico de La Plata preparó por primera vez la BCG. Actualmente, la producción de vacuna BCG en los laboratorios públicos fue discontinuada por una suma de factores. Por un lado hubo una disminución de la demanda por la reducción de dosis en los esquemas de vacunación pasando a aplicarse como dosis única en recién nacidos. Por otro lado, el precio de la vacuna BCG importada mediante mecanismos internacionales es menor al costo de su producción local. Sin embargo, las capacidades para producir BCG siguen presentes ya que actualmente se produce BCG Inmunoterapéutica, llamada también intravesical, para el tratamiento de cáncer de vejiga (Figura 2). Este producto es idéntico a la vacuna BCG con la diferencia en la concentración de la dosis, siendo cada dosis de BCG intravesical igual a 1200 dosis de la vacuna. La producción de BCG Inmunoterapéutica se realiza en el INPB y en el IBTP, los cuales cuentan con un stock de un lote semilla propio obtenido a partir de la cepa dinamarquesa Pasteur 1173 p2. La producción actual de BCG intravesical en el IBTP se realiza según normativa de la OMS, con habilitación de la PBA. El INPB cuenta con habilitación de ANMAT, basada en la norma ISO 9001:2008, aplicable a las normas Buenas Prácticas de Fabricación. Además, estos dos laboratorios producen un derivado proteico purificado (PPD) de M. tuberculosis que se utiliza en la reacción de Mantoux para el diagnóstico de la tuberculosis. La composición del PPD, denominado también tuberculina, es una mezcla de antígenos de la bacteria. El principio activo de la tuberculina se obtiene por precipitado por calentamiento del medio de cultivo de M. tuberculosis y filtración. La tuberculina está incluida en la lista de medicamentos esenciales de la Organización Mundial de la Salud.
El IBTP cuenta con una planta de Vacunas y Sueros que producía la Vacuna Doble Adulto Bacteriana (difteria-tétanos) hasta hace unos pocos años atrás, pero las capacidades para la producción de esta vacuna siguen presentes. El INPB dejó de producir vacunas bacterianas a finales de los años 90 (Corvalán, 2017), pero se mantuvo la capacitación de personal.
4.3 Vacunas bacterianas y derivados de bacterias
La vacuna viral antirrábica humana fue producida por muchos años tanto en el INPB como en el IBTP. El método utilizado se basaba en la extracción de virus de cerebros de ratón lactante e inactivación por radiación ultravioleta, que desnaturaliza el ácido nucleico y conserva la envoltura como antígeno inmunizante (Alarcón et al., 2018). Los animales de laboratorio que se utilizaban para la elaboración de esta vacuna y para el control de calidad eran criados en Bioterios propios. Esta metodología se dejó de utilizar por cuestiones de seguridad, ya que los virus obtenidos de células cerebrales contienen restos de membranas celulares que podrían provocar desmielinización. Esto llevó a la puesta en marcha de un proyecto entre el IBTP y la Universidad Nacional de La Plata para producir la vacuna antirrábica mediante cultivo celular. Como resultado se logró poner en funcionamiento la replicación del virus en cultivos de células BHK21, las cuales son aptas para producir la vacuna de uso veterinario (Figura 2). La planta de vacunas virales cuenta con un sector de cultivo, una zona de siembra, una zona de inspección y una zona de envasado y tiene habilitación del SENASA. Los procesos de producción se basan en botellas de vidrio denominadas “rollers” que permiten la producción de unas 200.000 dosis.
La fiebre hemorrágica argentina (FHA) es una patología de alta letalidad que surgió a comienzos de la década del ´50. Esta enfermedad se presenta solamente en una región del territorio argentino. El trabajo de médicos e investigadores argentinos llevó a la elaboración de una vacuna para prevenir la FHA, denominada Candid #1 (Ambrosio et al., 2006). El INEVH es el único productor de esta vacuna (Figura 2), contando con capacidades tecnológicas para producir vacunas virales a partir de cultivos de células animales. Candid #1 se produce utilizando técnicas de cultivos celulares con células FRhL-2 certificadas para multiplicar virus atenuados. La producción de la vacuna había sido discontinuada en el 2018 y fue retomada en el 2021 (Ministerio de Salud, 2021). La ANMAT aprobó el primer lote de la vacuna, con un total de 7771 viales, equivalente a 77.710 dosis. La vacuna Candid #1 pediátrica contra fiebre hemorrágica argentina (FHA) se encuentra actualmente en etapas de desarrollo.
4.4 Proteínas plasmáticas humanas
Las proteínas presentes en el plasma sanguíneo humano cumplen muchas funciones esenciales para el organismo. La albúmina sérica es la proteína más predominante, contribuyendo a mantener la presión oncótica del plasma y al transporte de lípidos y hormonas. Luego se encuentran las globulinas, que participan del transporte de iones, hormonas y lípidos y ayudan al sistema inmunológico. Finalmente, el fibrinógeno cumple un rol esencial en la coagulación de la sangre mediante su conversión en fibrina insoluble. Las proteínas plasmáticas restantes son enzimas, pro-enzimas y hormonas que se encuentran en muy baja proporción. Las proteínas plasmáticas de fabricación farmacéutica incluyen a la albúmina, concentrados de factores de coagulación e inmunoglobulinas. El uso terapéutico de las proteínas plasmáticas permite tratar diversas condiciones médicas y deficiencias como la Hemofilia, hemorragias, problemas de coagulación y trastornos de inmunodeficiencia, entre otros (Brodniewicz-Proba, 1991).
El primer fraccionamiento de plasma humano del Laboratorio de Hemoderivados fue realizado en 1972, a través del plan nacional de recuperación de plasma. La certificación internacional del primer lote oficial de albúmina se realizó en 1974 y unos años después se comenzó a producir gammaglobulina poliespecífica intramuscular (Massa 2003). La gammaglobulina endovenosa se sacó al mercado en 1997, la gammaglobulina antitetánica en 2001, el Factor VIII para el tratamiento de la hemofilia en 2005 y la Antitrombina III en 2006. Recientemente, fue autorizada por la ANMAT la elaboración y distribución de una gammaglobulina de administración subcutánea (Figura 2). El Laboratorio de Hemoderivados cuenta con dos plantas habilitadas por ANMAT para producción de estas proteínas plasmáticas. Para el fraccionamiento se utilizan técnicas de precipitación y separación por centrifugación o filtración, filtración tangencial e inactivación viral por temperatura. Una vez elaborado el producto se procede al envasado en viales y en los casos que se requiera se liofilizan las muestras. Todos los productos del LH cuentan con controles de procesos en los diferentes pasos, inspección de empaque una vez terminada la producción y análisis de control de calidad de lotes.
4.5 Desarrollo de nuevos biofármacos
Los laboratorios públicos cuentan también con capacidades actuales y proyectadas para desarrollar y producir nuevos biofármacos. A lo largo de los años se han llevado adelante diferentes proyectos de investigación y desarrollo en estos laboratorios, financiados por la Agencia I+D+i y por la ANLAP (Tabla 4).
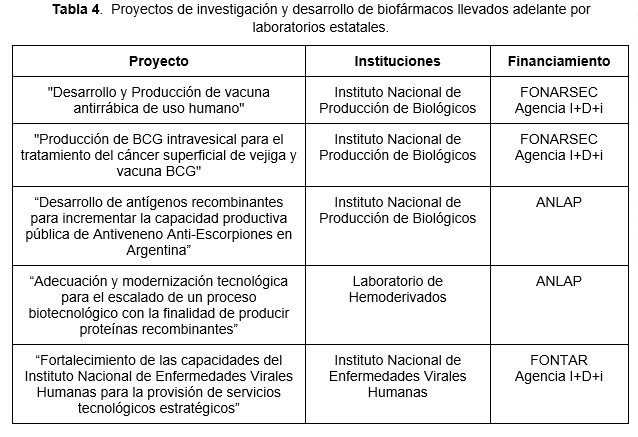
El Laboratorio de Hemoderivados lidera proyectos innovadores de alto impacto social, llevados adelante mediante una vinculación con la Universidad Nacional de Córdoba y el CONICET (Massa, 2013). La fuerte vinculación con grupos de investigación ha dado lugar a la puesta en marcha de diversos proyectos de investigación y desarrollo. Uno de estos proyectos, denominado BioHemo en sus orígenes, busca producir Factor IX recombinante para el tratamiento de la Hemofilia B. El desarrollo de la línea celular y del proceso de purificación fue realizado íntegramente en los laboratorios de investigación, obteniendo como resultado una proteína recombinante de alta pureza y con actividad biológica (Díaz de Guijarro, 2019). Este proyecto fue incorporado en el plan estratégico del laboratorio y se encuentra en marcha la puesta a punto de la producción a escala piloto, gracias al financiamiento otorgado por la ANLAP (Tabla 4). Si bien no se proyecta aún la etapa de producción industrial, cabe considerar que los volúmenes de dosis de Factor IX requeridas en nuestro país son reducidos y se podrán abastecer con la capacidad de la planta piloto. La planta de hemoderivados contará de esta manera con un sector de producción biotecnológica y podrá en un futuro diversificar la producción de biofármacos que se obtienen con cultivos de células CHO.
El proyecto titulado “Plataforma de antígenos recombinantes para el incremento de la capacidad productiva pública de antivenenos y antivirales”, presentado por ANLIS y la Facultad de Farmacia y Bioquímica de la UBA, es uno de los financiados por el FONARSEC PE-PMM 2021. Este tiene como objetivo la producción de componentes del veneno de la araña de rincón y del virus SARS-CoV-2 en larvas de insectos, para que sean utilizados como inóculo en la producción de anticuerpos en caballos y finalmente den lugar a antivenenos y antivirales. De esta manera, se busca reemplazar la inoculación de veneno con proteínas recombinantes, reduciendo la toxicidad y los efectos negativos en los animales.
La construcción de 3 nuevas plantas de vacunas en el Instituto Nacional de Producción de Biológicos cuenta con financiamiento de ANLIS y del FONARSEC (Pérez Ponsa et al., 2023). Los proyectos de investigación y desarrollo en curso son denominados “Producción de BCG intravesical para el tratamiento del cáncer superficial de vejiga y vacuna BCG” y “Desarrollo y producción de vacuna antirrábica de uso humano” (Tabla 4). El proyecto para la producción de BCG tiene como objetivo aumentar la capacidad productiva de BCG intravesical, desarrollar una forma farmacéutica liofilizada y desarrollar una formulación para la vacuna BCG. El proyecto para la producción de vacuna antirrábica tiene como objetivo el desarrollo de un producto de segunda generación para uso humano, elaborado por amplificación viral en cultivo de células y posterior inactivación química. Para esto se utilizará un cultivo de células VERO, línea celular ampliamente utilizada en la producción de vacunas virales humanas. Una vez concretadas las obras de las plantas, se podrá dar inicio inmediato a la producción de vacunas, gracias a que el laboratorio cuenta con los profesionales formados y entrenados (Know-How).
El proyecto entre el IBTP y la Universidad Nacional de La Plata para desarrollar la vacuna antirrábica para uso humano mediante cultivo en células Vero tuvo inicialmente financiamiento del FONARSEC PPM 2013 (Burgardt, González Maglio y Piñero, 2021). En un primer lugar se puso en funcionamiento la replicación del virus en cultivos de células BHK21, las cuales son aptas para producir la vacuna de uso veterinario. Actualmente está en curso un proyecto entre el IBTP y la Universidad Nacional de La Plata para producir la vacuna antirrábica mediante cultivo celular, replicando el virus en células BHK21. El proceso de producción actual se basa en “rollers” y se encuentra en desarrollo el proceso basado en reactores en suspensión de mayor capacidad. Una vez que este sistema se ponga a punto para la vacuna de uso veterinario se comenzará a optimizar la técnica de producción en rollers para cultivos de células Vero que permiten producir la vacuna antirrábica para uso humano.
Recientemente fue adjudicado un subsidio del MINCyT a través de la convocatoria de Centros de Desarrollo Tecnológico del Fondo Tecnológico Argentino (FONTAR) para el fortalecimiento de las capacidades del INEVH y la ampliación de sus instalaciones (I+D+i, 2022). Esta inversión se suma a los fondos otorgados por Nación para fortalecer las capacidades productivas del Instituto y volver a producir desde 2021 la vacuna Candid #1 contra la Fiebre Hemorrágica Argentina. El proyecto incluye la ampliación de la capacidad productiva en el INEVH que permitirá la prestación de servicios tecnológicos estratégicos en el campo de la salud humana, priorizando las enfermedades virales emergentes, especialmente las transmitidas por vectores y roedores pudiendo alcanzar una capacidad de 5000 viales hora. En particular serán impulsadas cuatro áreas de trabajo: 1. Fiebre Hemorrágica Argentina (FHA) y otros Arenavirus; 2. Hantavirus; 3. Dengue, Fiebre Amarilla y otros arbovirus; y 4. Producción de inmunobiológicos de importancia estratégica. La ampliación de la planta productora va a incorporar nuevos laboratorios y refuncionalizar parte de otros existentes, permitiendo llevar la producción de la vacuna Candid #1 a su capacidad máxima. La incorporación de un nuevo tren de llenado para la etapa de fraccionamiento de vacunas es un paso esencial para la producción, para el cual hay escasez de la oferta tanto en el país como a nivel global. Esto permitirá prestar servicios para la etapa terminal de la producción de vacunas y/o productos biotecnológicos. Además, será instalado un laboratorio con condiciones de Buenas Prácticas de Fabricación para la provisión de servicios de producción de Ingredientes Farmacéuticos Activos (IFA) y de lotes de vacunas destinadas a ensayos clínicos. Este laboratorio contará con biorreactores, una tecnología que permite la producción de sustancias bioquímicamente activas mediante cultivo de células. Los procesos en biorreactores permiten tener un control automatizado de inicio a fin del proceso, con altos rendimientos, muestreo seguro, condiciones de cultivo controladas y estandarización. Las capacidades para la prestación de servicios de ejecución de ensayos in-vitro e in-vivo de control de calidad de biológicos existentes en el INEVH serán modernizadas y ampliadas, incorporando un área de I+D+i para el desarrollo de nuevas tecnologías de producción de vacunas.
La importancia de los medicamentos para dar respuesta a las demandas de salud lleva a definirlos como un bien social, porque son imprescindibles para que los pacientes accedan a los tratamientos que necesitan. Cuando estos son comercializados por empresas privadas pueden darse situaciones que limitan el acceso a los mismos. Por ejemplo, dejan de ser producidos aquellos medicamentos que no son rentables en el mercado, no se desarrollan nuevos medicamentos para tratar las enfermedades que no son consideradas un buen negocio, y los medicamentos bajo patente se comercializan con precios excesivamente altos (Piñeiro, Chiarante y Zelaya, 2020). Para poder garantizar el acceso a los medicamentos los gobiernos deben encontrar maneras de solucionar estas problemáticas. La producción pública de medicamentos es una de las estratégias posibles para garantizar el abastecimiento de insumos sanitarios estratégicos. Su objetivo, cabe destacar, no es competir con los laboratorios privados, ya que en nuestro país contamos con un sector farmacéutico privado nacional amplio y diverso, que juega un papel importante en la economía. Entonces, los laboratorios públicos tienen la meta de producir los medicamentos que son requeridos por los agentes sanitarios o que son considerados estratégicos, siendo en muchos casos medicamentos que no se comercializan por empresas privadas.
El desarrollo exitoso de medicamentos requiere de un sistema de innovación y transferencia de tecnología maduro. Para esto hace falta contar con recursos humanos altamente especializados, fondos de financiamiento para las diversas etapas del desarrollo, conocimiento de las medidas regulatorias y de los mecanismos de transferencia de tecnología, empresas que apuesten a la innovación y políticas públicas que impulsen estos procesos. Cada eslabón es clave para lograr los resultados, no alcanza con el funcionamiento de alguno de ellos para que el desarrollo pueda ser finalmente aplicado exitosamente.
Los medicamentos biotecnológicos son utilizados en una amplia variedad de tratamientos y presentan un desafío para los Estados, ya que suelen ser productos de muy alto precio. Una de las estrategías para poder adquirir estos medicamentos a precios razonables fue la aplicación de políticas orientadas a fortalecer la producción de biológicos en el sector privado. Sin embargo, existen algunos biofármacos, como los de primera generación o los que no son rentables para el mercado, que podrían ser elaborados en el sector público para contribuir a garantizar la demanda del sistema de salud. Para impulsar la producción estatal de biofármacos es necesario contar con estudios de la complejidad técnica y de las capacidades productivas, así como también con la identificación de los productos biológicos estratégicos. En nuestro país hay una gran cantidad de grupos de investigación que cuentan con personal especializado en el desarrollo y la producción de moléculas biológicas, tanto a escala de laboratorio como a escala industrial. Varios de estos grupos han llevado adelante proyectos de transferencia tecnológica exitosos con laboratorios farmacéuticos privados y públicos (Lugones y Britto, 2020). En los últimos años, se pusieron en marcha obras y proyectos para la modernización de las plantas y los procesos productivos de los laboratorios estatales, con el objetivo de impulsar la producción de biofármacos. De esta manera, nuestro país cuenta con capacidades actuales y potenciales para la producción pública de biofármacos y vacunas esenciales.
El diseño e implementación de políticas y/o instrumentos que impulsen vínculos entre los laboratorios estatales y el sector científico-tecnológico es indispensable para fomentar el desarrollo y la producción de biofármacos con sentido social. La situación actual del país, con un gobierno que no está dando continuidad a las políticas de medicamentos, así como a las de ciencia y tecnología, significa la parálisis de cualquier proceso de desarrollo soberano. Si bien esto es claramente un retroceso, no necesariamente significa un freno para la producción en los laboratorios públicos. La trayectoria histórica demuestra la resiliencia de la PPM, la cual se sostuvo durante épocas adversas, sin el apoyo de la ANLAP o de políticas públicas. Incluso, el conocimiento adquirido por este sector durante los últimos años va a quedar resguardado en los laboratorios estatales así como los vínculos creados con diversos sectores científicos y productivos. Más tarde o más temprano, los obstáculos político-económicos que enfrenta la producción pública de biofármacos pueden ser superados.
Aguiar D.S., Fressoli M., Thomas H. (2007). Estilos socio-técnicos de producción de tecnologías conocimiento-intensivas: La conformación de una empresa de biotecnología en el campo de la salud humana en Argentina (1980-2006). Cuestiones de Sociología 4, 213-242.
Alarcón V., Pertierra V. R., Priani A., Aristizabal M., Vazquez T. (2018). Aporte del instituto biológico en el control de la rabia. Revista de Enfermedades Infecciosas Emergentes 13, 23-26.
Ambrosio A. M., Saavedra M. C., Riera L. M., Fassio R. M. (2006). La producción nacional de vacuna a virus Junin vivo atenuado (Candid #1) anti-fiebre hemorrágica argentina. Acta Bioquímica Clínica Latinoamericana 40(1), 5-17.
ANLAP (2023). Informe de gestión 2020-2023, Agencia Nacional de Laboratorios Públicos, Ministerio de Salud de la Nación.
Burgardt, N. I. (2022). Informe interno sobre Capacidades y Oportunidades para la Producción Pública de Productos Biológicos y Biosimilares. Agencia Nacional de Laboratorios Públicos, Ministerio de Salud de la Nación.
Burgardt N. I., González Maglio D., Piñero F. (2021). Investigación, Desarrollo y Producción Pública de Medicamentos: Análisis de Proyectos del Fondo de Innovación Tecnológica Sectorial de Salud. Primeras Jornadas CEUR | 60° aniversario Tecnología y Territorio: paradigmas tecno-económicos y nuevas configuraciones socio-espaciales en América Latina, 10-12 de noviembre de 2021, Ciudad de Buenos Aires, Argentina.
Brodniewicz-Proba T. (1991). Human Plasma Fractionation and the Impact of New Technologies on the Use and Quality of Plasma-derived Products. Blood Reviews 5, 245-257.
Casa Rosada (2018). La Argentina comenzará a producir una vacuna contra la fiebre amarilla. Casa Rosada, 11 de mayo de 2018. Recuperado (14/03/2024): https://www.casarosada.gob.ar/gobierno-informa/42687-la-argentina-comenzara-a-producir-una-vacuna-contra-la-fiebre-amarilla
Centeno A. (2016). Producción pública de medicamentos con sentido social. El Instituto Biológico Dr. Tomás Perón, pionero hace más de 50 años. Ciencia y Tecnología en la Provincia de Buenos Aires 1(1), 27-30.
CONETEC (2021). Informe Final “Proceso de Priorización para Evaluación de Tecnologías Sanitarias 2021”, Comisión Nacional de Evaluación de Tecnologías de Salud, Ministerio de Salud de la Nación.
Corvalán D. (2017). Des-Aprendizaje y Pérdida de Capacidades Locales. El Calendario Nacional de Vacunación en Argentina. Ciencia, Docencia y Tecnología 28(54), 1-37. Recuperado de: http://pcient.uner.edu.ar/cdyt/article/view/234
Díaz de Guijarro E. (2019). Laboratorio de Hemoderivados de Córdoba. Ciencia, tecnología y política 2(3), 030. DOI: https://doi.org/10.24215/26183188e030
Fan H. W., Vigilato M. A. N., Pompei J. C. A., Gutiérrez J. M. (2019). Situación de los laboratorios públicos productores de antivenenos en América Latina. Revista Panamericana de Salud Pública 43, e92. DOI: https://doi.org/10.26633/RPSP.2019.92
García S., Antolini L., Hass A. I., Martín M. L., Penna A. M., Yanicelli M. T. (2011). Guía de Centros Antiponzoñosos de la República Argentina. Programa Nacional de Prevención y Control de las Intoxicaciones, Ministerio de Salud de la Nación.
Gollán D. (2024). Impacto del DNU 70/23 en el sistema de salud. Soberanía Sanitaria. Recuperado (9/05/2024): https://revistasoberaniasanitaria.com.ar/impacto-del-dnu-70-23-en-el-sistema-de-salud/
Gutman G., Lavarello P. y Pita J. J. (2020). Política Industrial en la Industria Biofarmacéutica: Nuevos (y Renovados) Desafíos Frente COVID-19. Portal Instituto Argentino para el Desarrollo Económico-Realidad Económica.
Gutman G., Lavarello P. y Pita J. J. (2021). Elementos de diagnóstico y lineamientos generales para una política de promoción de biosimilares en Argentina. Documentos de Trabajo del Consejo para el Cambio Estructural N° 4, Ministerio de Desarrollo Productivo de la Nación.
Instituto Biológico Dr. Tomás Perón (2019). Manual de Calidad. Versión 3. Dirección Provincial del Instituto Biológico “Dr. Tomás Perón”. IF-2019-30595604-GDEBA-DPIBDTPMSALGP. Recuperado (14/0/.2024): https://www.ms.gba.gov.ar/sitios/institutobiologico/files/2019/09/V.3.-IF-2019-30595604-GDEBA-DPIBDTPMSALGP.pdf
I+D+i (2021). Convocatoria Proyectos Estratégicos en Producción Pública de Medicamentos (PE PPM). Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i).
I+D+i (2022). Incremento y fortalecimiento de las capacidades del Instituto Nacional De Enfermedades Virales Humanas (INEVH) para la provisión de servicios tecnológicos estratégicos (CEN-TEC-2022-003, Resolución 138/2022). Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i).
Isturiz M. A., Díaz de Guijarro E., Naidorf J. (2018). Producción Pública de Medicamentos, Vacunas y Productos Médicos. El Papel de las Universidades. Revista de la Asociación Argentina de Sociología 10(6), 97-112.
Lavecchia G. (26 de diciembre de 2023). Kicillof impulsa la creación del Centro de Industria Farmacéutica Bonaerense. Tiempo Argentino. Recuperado (14/03/2024): https://www.tiempoar.com.ar/ta_article/kicillof-impulsa-la-creacion-del-centro-de-industria-farmaceutica-bonaerense/
Lugones G. E., Britto F. A. (2020). Bases y determinantes para una colaboración exitosa entre ciencia y producción. Ciudad Autónoma de Buenos Aires: CIECTI.
Massa C. (2013). 50 años de compromiso con la vida. Laboratorio de Hemoderivados de la Universidad Nacional de Córdoba. Córdoba: Editorial de la UNC.
Matar P. (2017). ¿Qué significa biosimilaridad? Capítulo 2. González-Andrade F. (ed.). Medicamentos biológicos, presente y futuro de la terapéutica. Quito: Facultad de Ciencias Médicas, Universidad Central del Ecuador.
Ministerio de Ciencia, Tecnología e Innovación Productiva (2012). Plan Argentina Innovadora 2020, Ministerio de Ciencia y Tecnología.
Ministerio de Defensa (2021). Rossi recorrió las obras de modernización del Laboratorio Farmacéutico Conjunto que amplían las capacidades de producción, Portal del Ministerio de Defensa. Recuperado de: https://www.argentina.gob.ar/noticias/rossi-recorrio-las-obras-de-modernizacion-del-laboratorio-farmaceutico-conjunto-que-amplian
Ministerio de Salud (2021). Luego de tres años, el país vuelve a producir la vacuna contra la Fiebre Hemorrágica, Portal del Ministerio de Salud de la Nación. Recuperado de:
https://www.argentina.gob.ar/noticias/luego-de-tres-anos-el-pais-vuelve-producir-la-vacuna-contra-la-fiebre-hemorragica
Montelongo-Jauregui D., Vila T., Sultan A. S., Jabra-Rizk M. A. (2020). Convalescent serum therapy for COVID-19: A 19th century remedy for a 21st century disease. PLOS Pathogens 16(8): e1008735. DOI: https://doi.org/10.1371/journal.ppat.1008735
OMS (1991). Good Manufacturing Practices for biological products. TRS no 822, Annex 1, Organización Mundial de la Salud. Recuperado de (14/03/24): https://www.who.int/biologicals/areas/en/
Ortiz-Prado E., Ponce-Zea J., Vasconez JE, Castillo D., Checa-Jaramilloz D. C., Rodríguez-Burneo N., Andrade F., Intriago-Baldeón D. P., Galarza-Maldonado C. (2020). Current trends for biosimilars in the Latin American market. Generics and Biosimilars Initiative Journal 9(2):64-74. DOI:10.5639/gabij.2020.0902.011
Pérez Ponsa M. E., Antón E., Burgardt N. I., Wilhelm C., Chiarante N. (2023). “Informe sobre Capacidades Públicas en investigación, desarrollo y producción de vacunas estratégicas en Argentina”, Agencia Nacional de Laboratorios Públicos, Ministerio de Salud de la Nación.
Piñeiro F., Chiarante N., Zelaya M. (2020). Sobre la investigación, desarrollo y producción pública de nuevos medicamentos. Ciencia, Tecnología y Política 3(4), 83-90.
Sánchez M. L. (2020). Biofármacos. Bioquímica y Patología Clínica 84(3), 44-51.
Zelaya M., Burgardt N., Chiarante N., Piñeiro F., Alcain J., González Maglio D. y Carro A. C. (2021). Producción Pública de Medicamentos y Vacunas: análisis histórico y de políticas científicas con foco en el caso argentino. Filosofía e historia de la ciencia y sociedad en Latinoamérica; Volumen I, 173-200, Buenos Aires y São Carlos, AFHIC.

